Guri Hagberg, lege i spesialisering, PhD-stipdenidat, Bærum sykehus, Vestre Viken HF
Håkon Ihle-Hansen, lege i spesialisering, Phd-Stipendiat, Bærum sykehus, Vestre Viken HF
Hege Ihle-Hansen, Overlege, Phd, Bærum sykehus, Vestre Viken HF
Tiden som går frem til riktig behandling er helt avgjørende for godt utkomme etter iskemiske hjerneslag. De siste par årene har syv randomiserte kontrollerte studier (RCT’er) vist gevinst av trombektomi, i kombinasjon med trombolyse, hos et selektert utvalg av slike pasienter. Alle som jobber i helsevesenet må kunne gjenkjenne bortfall av funksjon som symptom på mulig hjerneslag og handle deretter.
 Resultat i hjerneslagstudier
Resultat i hjerneslagstudierNår man skal vurdere om en behandling har effekt ved hjerneslag, brukes ofte Modified Rankin Scale, mRS [1]. Dette er en skala for funksjonsgradering ved hjerneslag, med skår fra 0 til 6 (Figur 1).
I trombolysestudiene har et godt utkomme vært definert som mRS 1 eller bedre. Ved de nye studiene som inkluderer trombektomi er nå mRS 2 eller bedre definert som et godt utkomme. Mens mRS er et mål for global funksjon, brukes National Institutes of Health Stroke Scale (NIHSS) for kartlegging av nevrologiske utfall [2]. NIHSS vurderer hjerneslagets effekt på nivå av bevissthet, språk, neglekt, synsutfall, øyebevegelser, kraft, koordinasjon og førlighet. NIHSS må tolkes med forsiktighet, da man i studier har sett at skalaen er vektet mer mot slag i forsyningsområdet til det fremre kretsløpet, og at det er dårlig samsvar mellom NIHSS og grad og lokalisasjon av okklusjon [3, 4].
Kunnskapsgrunnlaget for at trombolyse er god behandling ved akutt iskemisk hjerneslag har vi hatt i mange år. Det er nå over 20 år siden de første studiene kom, og intravenøs (iv) behandling med alteplase ble godkjent som basalbehandling i Norge i 2003. I 2014 ble det publisert en meta-analyse i Lancet [5], som viser at tid fremdeles er svært viktig for å få effekt av behandling (figur 2), og at trombolyse ikke gir mer blødninger og er effektivt også hos pasienter over 80 år og de med lette slag, dvs. NIHSS 0-4 (figur 3).
Meta-analysen baserer seg på 9 RCT’ er med totalt 6756 pasienter. Tallene viser at hvis vi starter trombolyse innen 60 min etter symptomdebut må 2-3 behandles for at en pasient skal ha effekt. Går det 4,5 timer må 15-12 behandles.

Figur 2: Effekt av tid til alteplasebehandling på godt utkomme. Fra Emberson et.al, Lancet 2014; 384(9958):1925-35, trykkes med tillatelse.
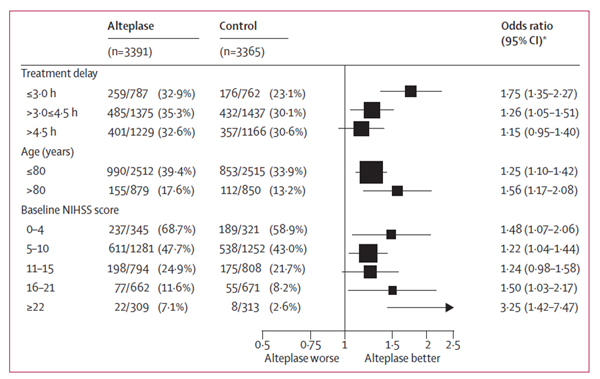
Figur 3: viser effekt av alteplase i subgrupper inndelt etter tid fra symptomdebut, pasientens alder og NIHSS-skår. Odds Ratio angir sannsynligheten for et godt utkomme (mRS 0-1) ved trombolyse kontra placebo ved forsinket behandling, høy alder og høy NIHSS-skår. Det er økt sannsynlighet for et godt utkomme ved trombolyse i alle subgrupper i studien. Tallene indikerer også at noen kan ha nytte av trombolyse utover dagens tidsvindu på 4,5 timer fra symptomdebut. Studien viser også at det er en økt risiko for hjerneblødning etter trombolysen (6,8 %), men man fant ingen forskjell i 90 dagers mortalitet. Fra Emberson et.al, Lancet 2014; 384(9958):1925-35, trykkes med tillatelse.
Denne kunnskapen har heldigvis ført til endringer i sykehus som mottar pasienter med hjerneslag. Trombolysealarm, der lege, bioingeniør, sykepleier og radiolog samtidig varsles, er blitt en rutine hos de fleste. Målet er raskt å stille korrekt diagnose, utelukke kontraindikasjoner og starte trombolyse for re-etablering av cerebral sirkulasjon så raskt som mulig. Det er et økt fokus på akutt hjerneslagsbehandling, og flere unge som eldre kolleger må og vil lære mer om hjerneslag. Tallene fra Norsk hjernelagsregister 2014 viser at vi gjør en god jobb, men at det finnes et forbedringspotensiale, særlig når det gjelder å komme raskt nok til sykehus [6].
 Det ble i 2014 innrapportert 8409 hjerneslag til registeret (Tabell 1). 51 av 54 sykehus som behandler hjerneslag oppga data, men med varierende dekningsgrad. Med dekninggrad menes andelen av det totale antall hjerneslag som rapporteres til registeret. Sykehus med en dekningsgrad på under 70 % er ikke tatt med i videre analyser i årsrapporten. Tallene viser at 80 % av pasientene med hjerneslag er over 65 år, og at 64 % har en NIHSS fra 0-5. Den tidligere nevnte meta-analysen synes derfor overførbar til norske forhold.
Det ble i 2014 innrapportert 8409 hjerneslag til registeret (Tabell 1). 51 av 54 sykehus som behandler hjerneslag oppga data, men med varierende dekningsgrad. Med dekninggrad menes andelen av det totale antall hjerneslag som rapporteres til registeret. Sykehus med en dekningsgrad på under 70 % er ikke tatt med i videre analyser i årsrapporten. Tallene viser at 80 % av pasientene med hjerneslag er over 65 år, og at 64 % har en NIHSS fra 0-5. Den tidligere nevnte meta-analysen synes derfor overførbar til norske forhold.
Tabell 2 gir et bilde av trombolysepraksis i Norge 2014. 16 % av hjerneslagspasientene fikk trombolyse, noe som er nært opp til myndighetenes mål om 20 %. 43 % av pasientene hadde lette slag, d.v.s. NIHSS 0-5. Pasienter over 80 år fikk trombolyse på lik linje med de under 80 år. 57 % ble trombolysert innen 40 min etter ankomst sykehus. Dessverre ser vi at det fremdeles var 40 % som kom for  sent til sykehus og ikke kunne motta trombolyse med dagens behandlingsvindu på 4,5 timer.
sent til sykehus og ikke kunne motta trombolyse med dagens behandlingsvindu på 4,5 timer.
Enkelte sentre har rutinemessig drevet med endovaskulær behandling helt siden PROACT-studien ble publisert i 1999 [7]. Denne studien viste at det gikk bedre med de som fikk intraarteriell kateterbasert trombolyse i kombinasjon med iv heparin ved sentrale media-okklusjoner sammenlignet med heparin gitt alene. Utviklingen av endovaskulær behandling fra intraarteriell kateterbasert trombolyse til dagens trombektomi ved bruk av stent-retrivere med sug, har gått tregt grunnet usikkerhet rundt effekt og riktig pasientseleksjon. I 2013 ble det publisert 3 studier som viste at endovaskulær behandling ikke var bedre enn trombolyse gitt alene, men da uten forbehandling med trombolyse.
Mot slutten av 2014 og i løpet av 2015 ble det imidlertid publisert hele 7 RCT’er, som alle viste bedre utkomme ved en kombinasjon av trombolyse og trombektomi, sammenlignet med trombolyse alene, for et lite utvalg av pasientene [8-13]. Bedre billeddiagnostikk, som fører til riktigere utvelgelse av pasienter, samt nye stentretrivere med mekanisk sug har blitt nevnt som viktige årsaker til gjennombruddet.
Tabell 3 er en oppstilling av enkelte relevante data tilgjengelige fra studiene. Alle studiene hadde inklusjonskriteriet om påvist okklusjon i proksimale del av arteria cerebri media. Det var kun MR CLEAN, en nederlandsk multisenterstudie som inkluderte pasienter fra 2010- 2014, som rakk å oppnå sitt mål om 500 inkluderte. De andre ble stoppet underveis etter sikkerhetsanalyser grunnet klar fordel for intervensjonsgruppen, med number needed to treat (NNT) på 3-7. Pasientene i studiene er i gjennomsnitt 10 år yngre enn pasientene i Norsk hjernelagsregister, de har store hjerneslag med høy NIHSS-skår som uttrykk for sentrale tromber i de store blodårene i hjernen, og det er kort tid fra symptomdebut til intervensjon. Mortaliteten varierer mellom de ulike studiene der MR CLEAN har 21 % og EXTEND IA har 9 %. Slike forskjeller kan skyldes at man i EXTEND IA hadde strenge krav til deltagende sentra med tanke på antall intervensjoner årlig. EXTEND IA, en australsk multisenterstudie, hadde også noe strengere inklusjonskriterier enn MC CLEAN da infarktkjernen skulle være var mindre (<70 ml).
Det foreligger nå en svak anbefaling for trombektomi i European Stroke Organisation (ESO) guidelines fra mai 2015 [14]. For pasienter med okklusjon i intra-cranielle del av ICA (arteria karotis interna) eller proksimalt i MCA (arteria cerebri media), med liten infarktkjerne og tilstrekkelig kollateral sirkulasjon, vil rask endovaskulær behandling, etter iv trombolyse og innen 6 timer, gi bedre mRS og redusere mortalitet. Ved andre okklusjoner eller ved kontraindikasjoner for trombolyse må behandlingen fremdeles anses som eksperimentell.
Det er også lansert en internasjonal anbefaling om at et intervensjonssenter må ha 1 million mennesker i sitt nedslagsfelt, minimum 500 slagpasienter og minst 60 intervensjoner årlig (European Society of Minimally Invasive Neurological Therapy (ESMINT)). Overført til norske forhold vil dette kun gjelde hovedstadsområdet, så løsninger for å sikre god kompetanse må opprettes.
En forutsetning for god behandling er riktig seleksjon av pasientene. I en artikkel skrevet av Geir Ringstad og Eva Jacobsen ved nevroradiologisk enhet, Oslo Universitetssykehus (OUS), Rikshospitalet i august 2015 for norsk radiologisk forening skisseres kompetansen som kreves døgnet rundt for å kunne tilby en forsvarlig og god tjeneste [15]. Det er ved hjelp av MR, evt. CT- diffusjon og perfusjon, mulig å kartlegge penumbra og kollateral sirkulasjon. Dette, sammen med en god vurdering av en kliniker, gjør det mulig å selektere de pasientene som er aktuelle for behandling. I tillegg kreves nærhet til nevrokirurg grunnet mulige komplikasjoner under inngrepet. Det foregår mye forskning på feltet nevroradiologi og mulighet for forlenget tidsvindu.
Antall endovaskulære intervensjoner som utføres i Norge, eller hvor mange som opplever komplikasjoner i tilknytning til prosedyren, er noe usikkert. For 2014 var det 82 innrapporterte trombektomier i Norsk hjerneslagsregister, noe som utgjør 1 % av pasientene. Ved Stavanger universitetssykehus viser tall fra de senere år at 3-5 % av slagpasientene fikk endovaskulær intervensjon, svarende til 20 pasienter i 2014 [16]. Det utføres trombektomi ved alle universitetssykehusene i Norge, og en uformell datainnsamling tyder på at 100 pasienter gjennomgikk trombektomi i 2014 [17]. Det er vanskelig å anslå hvor mange pasienter som potensielt kan være aktuelle for trombektomi i fremtiden, men basert på dagens forskningsresultater er det få pasienter som er aktuelle.
Norge har, i tillegg til lavt volum, også noen geografiske utfordringer som ikke gjør de nye studiene direkte overførbare. En oversikt over avstander mellom universitetssykehus og lokalsykehus i Norge viser at trombolysebehandling enkelte steder må starte lokalt før man vurderer overflytning til et regionalt senter. For enkelte områder blant annet i Troms, Finnmark og Svalbard vil man i dag ikke kunne nå et senter som utfører trombektomi i tide [18].
En uoffisiell opptelling av pasienter meldt til akuttmottaket med mulig cerebral hendelse en tilfeldig høstuke på Bærum Sykehus, Vestre Viken i 2015, viser viktigheten av bred indremedisinsk og nevrologisk kompetanse i møte med pasientene. Trombolysealarmen utløses når sykehistorien indikerer at trombolyse kan bli aktuelt, og gjøres oftest i samråd med vakthavende lege. Denne uken ble det meldt 21 pasienter med tentativ innleggelsesdiagnose cerebral hendelse. Det ble utløst 5 trombolysealarmer. Av de 5 fikk 2 trombolyse, 2 kom for sent og 1 viste seg å være Parkinson med on-off symptomer. 16 av 21 pasienter viste seg å feile noe annet enn cerebral hendelse. Infeksjon, migrene, alkoholintox, hypotensjon grunnet overbehandling med antihypertensiva og angst var noen av diagnosene pasientene hadde.
Figur 6 gir en oversikt over viktige differensialdiagnoser som må utelukkes. Feildiagnostikk vil ha betydning for prognosen. En rask somatisk undersøkelse samt måling av blodtrykk, puls, temperatur, respirasjonsfrekvens og blodsukker, er som regel tilstrekkelig i akuttfasen.
I en studie publisert fra Akershus Universitetssykehus (Ahus) i 2005, så man at 25 % av pasientene som ble innlagt på slagavdelingen for mistenkt hjerneslag hadde en annen diagnose [19].
Denne vanskelige akuttdiagnostikken gjør direkte transport til et endovaskulært senter meget komplisert. Det finnes ikke et prehospitalt diagnostisk verktøy, som med tilstrekkelig grad av presisjon, kan angi om det foreligger en cerebral hendelse eller ikke. Dette, i motsetning til ved hjerteinfarkt, der spesifikke forandringer i EKG brukes som et slikt verktøy.
I tillegg til acetylsalisylsyre i metningsdose, og iv trombolyse så raskt som mulig, er innleggelse og videre behandling i slagenhet evidensbasert medisin ved iskemisk hjerneslag [20]. Muligheter for trombektomi til noen få må ikke forsinke trombolyse eller innleggelse på en dedikert slagenhet for flertallet.
I Nasjonale faglig retningslinje for behandling og rehabilitering ved hjerneslag, er det grundig beskrevet hva som kreves av et tverrfaglige spesialopplært personale i en slagavdeling. Innleggelese i løpet av 24 timer i en slagavdeling er et av kvalitetsmålene i Norsk Hjerneslagregister. Lege, slagsykepleier, fysioterapeut, ergoterapeut og logoped har alle definerte ansvars- og kompetanseområder, som er viktige for et optimalt pasientforløp.
Det foregår i dag mye spennende når det gjelder behandling av hjerneslag i Norge. Basert på den nye kunnskapen har det oppstått et behov for gjennomgang av dagens praksis, og vurdering av mulig reorganisering. Det kommer nye nasjonale retningslinjer for hjerneslag i løpet av 2016, og det vil komme pakkeforløp for hjerneslag. Pakkeforløpet skal sikre lik behandling for flest mulig til riktig tid. Det er sannsynlig at man i fremtiden vil definere ulike slagsentre som primære og regionale i større grad enn man har gjort tidligere, men at hensynet til flertallet av pasientene gjør en generell sentralisering i Norge uaktuell. Det er også kommet forslag om en egen spesialisering for slagleger, og det er opprettet en egen norsk slagorganisasjon, NSO, Norwegian Stroke Organisation.
Tallene fra Norsk hjerneslagsregister viser at mange kommer for sent til trombolyse, og at det er behov for en ensartet nasjonal informasjonskampanje. I tillegg pågår det stadig spennende forsking i Norge som vil kunne forbedre slagbehandlingen fremover, både når det gjelder akuttbehandling, i slagenheten og i rehabiliteringsfasen. Geriatrien er for mange en inngangsport til slagmedisinen. Den geriatriske arbeidsmodellen med bredt perspektiv og involvering av mange ulike yrkesgrupper tilfredsstiller mange av kravene i den komplekse oppfølgingen en pasient med hjerneslag trenger. Kombinasjonen av utfordrende akutt diagnostikk og teamarbeid tiltrekker seg mange nye unge kollegaer, og er veien å gå for fremtidens geriatri, sykehus og slagmedisin.