Demografien i Norge er i endring. Med en jevn økning av eldre, vil andelen eldre > 75 år anslagsvis øke med 100% innen 2040 (1). Prevalensen av atrieflimmer (AF) er relativt høy blant eldre personer, ca 10% ved 75 års alder, sammenlignet med 2% i den generelle befolkningen (2). Med økende alder øker også antall pasienter med AF og behovet for antikoagulasjon. Den økende bruk av antikoagulasjon er illustrert i tabell 1.
I dag behandles totalt ca 140 000 pasienter i Norge med antikoagulantia, og pågående antikoagulasjonsbehandling ved akutte sykehusinnleggelser er assosiert med økt risiko for blødning og komplikasjoner, forlenget sykehusopphold, forsinket kirurgi, samt prematur død (4). Det er særlig to hovedgrupper av pasienter på antikoagulasjonsbehandling, som kan ha behov for akutt normalisering av hemostase:
1) Pasienter med behov for akutt kirurgi (f.eks. etter fraktur eller ulykke) eller akutt invasiv prosedyre (f.eks. behov for pacemaker), som ifølge internasjonal litteratur gjelder ca. 2% årlig (3-8).
2) Pasienter som utvikler alvorlig blødning (f.eks. hjerneblødning eller gastrointestinal blødning) relatert til bivirkninger av antikoagulantia, som i henhold til studier gjelder ca. 1,5% årlig (figur 1) (6-8).
3,5% av totalt 140 000 pasienter på antikoagulasjon i Norge, hvorav 80 000 pasienter på NOAK, utgjør et ikke ubetydelig antall pasienter som kan ha behov for akutt normalisering av hemostase, hhv. ca. 4 900 og 2 800 pasienter per år (Figur 1).
I dag behandles totalt ca 140 000 pasienter i Norge med antikoa-gulantia, og pågående antikoagu-lasjonsbehandling ved akutte sykehusinnleggelser er assosiert med økt risiko for blødning og komplikasjoner, forlenget sykehusopphold, forsinket kirurgi, samt prematur død (4). Det er særlig to hovedgrupper av pasienter på antikoagulasjonsbehandling, som kan ha behov for akutt normalisering av hemostase:
1) Pasienter med behov for akutt kirurgi (f.eks. etter fraktur eller ulykke) eller akutt invasiv prosedyre (f.eks. behov for pacemaker), som ifølge internasjonal litteratur gjelder ca. 2% årlig (3-8).
2) Pasienter som utvikler alvorlig blødning (f.eks. hjerneblødning eller gastrointestinal blødning) relatert til bivirkninger av antikoagulantia, som i henhold til studier gjelder ca. 1,5% årlig (figur 1) (6-8).
3,5% av totalt 140 000 pasienter på antikoagulasjon i Norge, hvorav 80 000 pasienter på NOAK, utgjør et ikke ubetydelig antall pasienter som kan ha behov for akutt normalisering av hemostase, hhv. ca. 4 900 og 2 800 pasienter per år (Figur 1).
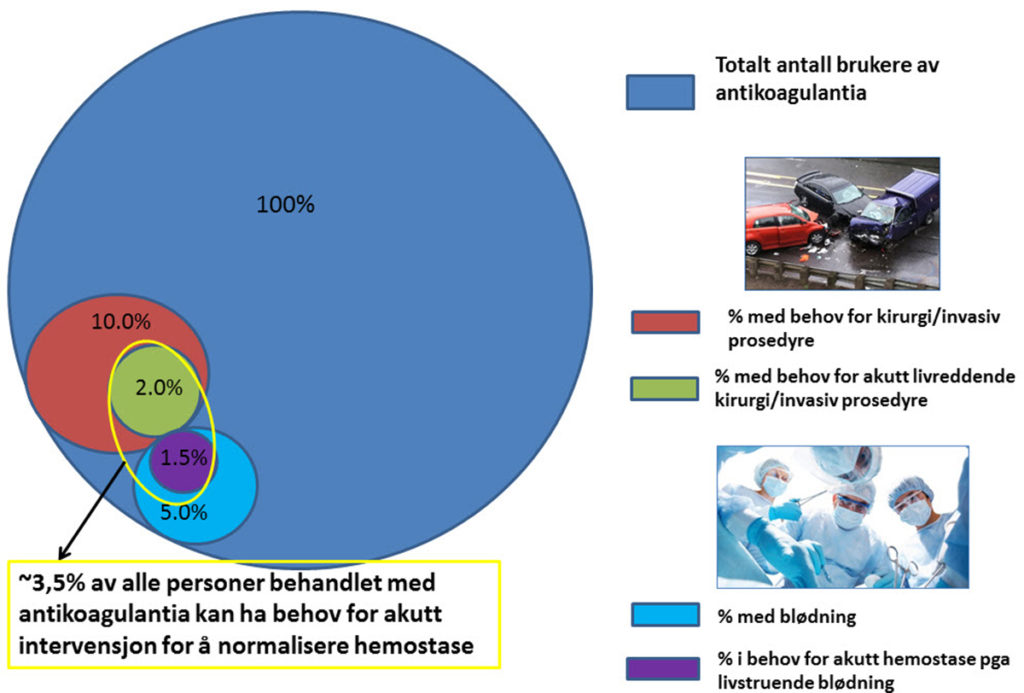
Figur 1. Illustrasjon i andel pasienter behandlet med antikoagulasjon årlig som potensielt kan ha behov for umiddelbar normalisering av hemostase. både nasjonalt og internasjonalt.
Ved behov for øyeblikkelig reversering av vitamin K-antagonister (warfarin) sin effekt, benyttes i dag hovedsakelig inaktivert protrombinkonsentrater PCC (octaplex, beriplex, prothroplex) eller octaplas. Effekten av disse behandlingsalternativene er uklar i forhold til å begrense blødning, da veldig få studier har studert dette prospektivt (9,10). Administrering av vitamin K, som et middel for å reversere effekten ved å gjenopprette normal syntese av de vitamin K-avhengige koagulasjonsfaktorene gir ingen akutte effekter da denne effekten inntrer sent (ofte etter 12-24 timer), men benyttes i klinikken i mangel av andre alternativer.
NOAKs er i utbredt bruk som primær- og sekundærprofylakse av embolisk slag blant voksne pasienter med ikke-klaffeassosiert AF med én eller flere risikofaktorer. Andre indikasjoner omfatter behandling av venøs trombose og tromboseprofylakse ved kne-/hofteprotesekirurgi.
Håndtering av alvorlige blødninger hos pasienter som behandles med NOAK har frem til nå vært relativ lik som hos pasienter behandlet med vitamin K-antagonister, bortsett fra at vitamin K ikke gis (10). Seponering av antikoagulasjonsbehandlingen, bruk av mekanisk kompresjon, tilførsel av plasma- og/eller blodprodukter (erytrocytter, trombocytter) eller behandling med protrombinkompleks-konsentrat («PCC», f.eks Prothromplex, Octaplex eller Confidex) eller aktivert PCC (aPCC) (f.eks Feiba) kan være aktuelt. Studier vedrørende protrombinkonsentrater og NOAK er begrenset til dyreforsøk og studier på friske frivillige (10). Hos stabile pasienter på dabigatran kan også hemodialyse vurderes (11).
Grunnet relativt kort halveringstid av NOAK, forutsatt normal nyrefunksjon (tabell 2), har tradisjonelt ekspektans vært utøvet ved semi-akutte tilstander. Ettersom tidsaspektet er viktig, særlig ved høy-risiko kirurgi, er imidlertid dette problematisk for alle NOAK-klasser og tilgjengeligheten av en spesifikk antidot vil da kunne være avgjørende.
Et middel som nå er tilgjengelig og som umiddelbart opphever antikoagulasjonseffekten spesifikt for et av de tilgjengelige NOAKs (dabigatran), er idarusizumab (Praxbind).
Idarusizumab er et humanisert monoklonalt antistoffragment som har blitt spesifikt utarbeidet som et reverserende middel for dabigatran. Det fasiliterer umiddelbar, fullstendig og vedvarende (minst 12 timer) normalisering av hemostase ved å binde fritt og trombinbundet dabigatran (12), med en affinitet som er ca. 350 ganger høyere enn for bindingen av dabigatran til trombin (Figur 2).
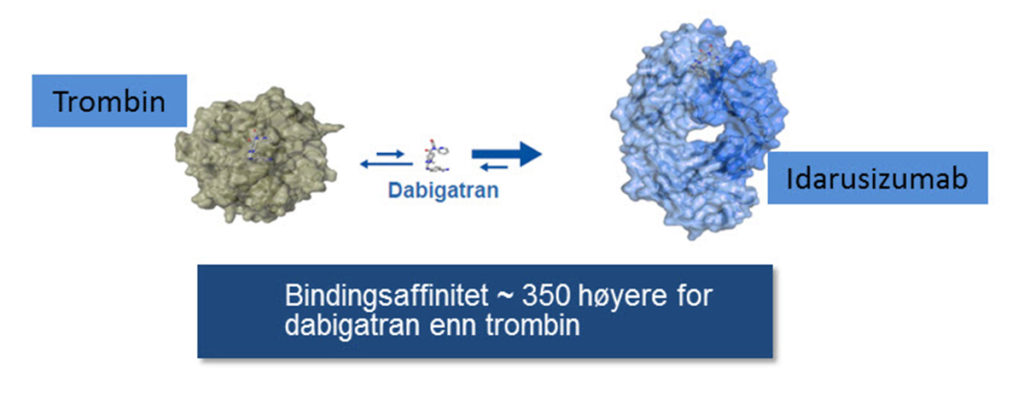
Figur 2. Skjematisk illustrasjon av idarusizumabs virkningsmekanisme (omarbeidet fra Schiele et al. A specific antidote for dabigatran: functional and structural characterization. Blood 2013;121:3554-62).
Idarusizumab er spesifikk for dabigtran og har til nå ikke vist protrombotiske eller plateaktiverende effekter. Den farmakologiske effekten av idarusizumab er dose-avhengig, karakteriseres ved rask binding og langsom dissosiasjon fra dabigatran, hvilket er typisk for en høy-affinitets-binding. Dette innebærer i praksis en tilnærmet irreversibel binding, og dermed et stabilt idarusizumab-dabigatran kompleks. Blant friske frivillige oppnås maksimal konsentrasjon av idarusizumab etter 5 minutter infusjon.
Idarusizumab (Tabell 3) ble anbefalt tatt i bruk av Beslutningsforum 14. mars 2016 (13). Legemiddelet er i dag tilgjengelig på de fleste norske sykehus og har allerede blitt benyttet ved ulike akutte situasjoner, som bl.a. hofteoperasjon, gastrointestinal (GI) blødning, hjerneblødning og for behandling før trombolysebehandling av iskemisk hjerneinfarkt.
Studien som ligger til grunn for godkjenning av idarusizumab er fase III-studien RE-VERSE AD™ (study of the REVERSal of Effects of idarucizumab in patients on Active Dabigatran), som totalt inkluderte 503 pasienter (12, 14, 15). Fem norske sykehus (Tromsø, Haukeland, Ullevål, Drammen og Østfold) har deltatt i studien med totalt 13 pasienter. Studien har en åpen design, og inkluderte pasienter behandlet med dabigatran med ukontrollerte eller livstruende blødninger (gruppe A, n=298) eller med behov for akutt kirurgi eller invasive prosedyrer (gruppe B, n=196) (16). Dette inkluderer alvorlig syke eller skadde pasienter (f.eks. pasienter i trafikkulykker med omfattende skader, pasienter med aortaaneurisme, pasienter som trenger akutt implantasjon av pacemaker eller med GI blødning) (12, 14, 15).
Det primære endepunktet for studien, reversering av den antikoagulerende effekten av dabigatran innen fire timer ble målt som fortynnet trombintid (dTT) og «ecarin clotting time» (ECT; en laboratorietest for å måle aktiviteten av direkte trombinhemmere) (14, 15), og ble oppnådd for 100 % av pasientene.
Som sekundære kliniske endepunkt, ble i tillegg følgende evaluert:
1) Hvorvidt det under prosedyren eller inngrepet forelå normal hemostase i gruppe B (d.v.s. pasienter med behov for akutt kirurgi eller invasive prosedyrer). 93% av operatørene rapporterte dette.
2) Tid til klinisk blødningsstopp i gruppe A (d.v.s. pasienter behandlet med dabigatran med ukontrollerte eller livstruende blødninger), som ble rapportert til 3,5 – 4,5 timer. Det ble ikke gjort observasjoner som utløste bekymring angående sikkerhet eller bivirkninger knyttet til bruken av idarusizumab, og kun få pasienter (1,4%) trengte mer enn 5 g administrasjon av medikamentet for å oppnå normalisering av hemostase.
Antidotet er nå også inkludert i en anbefalt behandlingsstrategi for håndtering av blødning for pasienter under antikoagulasjonsbehandling (Figur 3) (10).
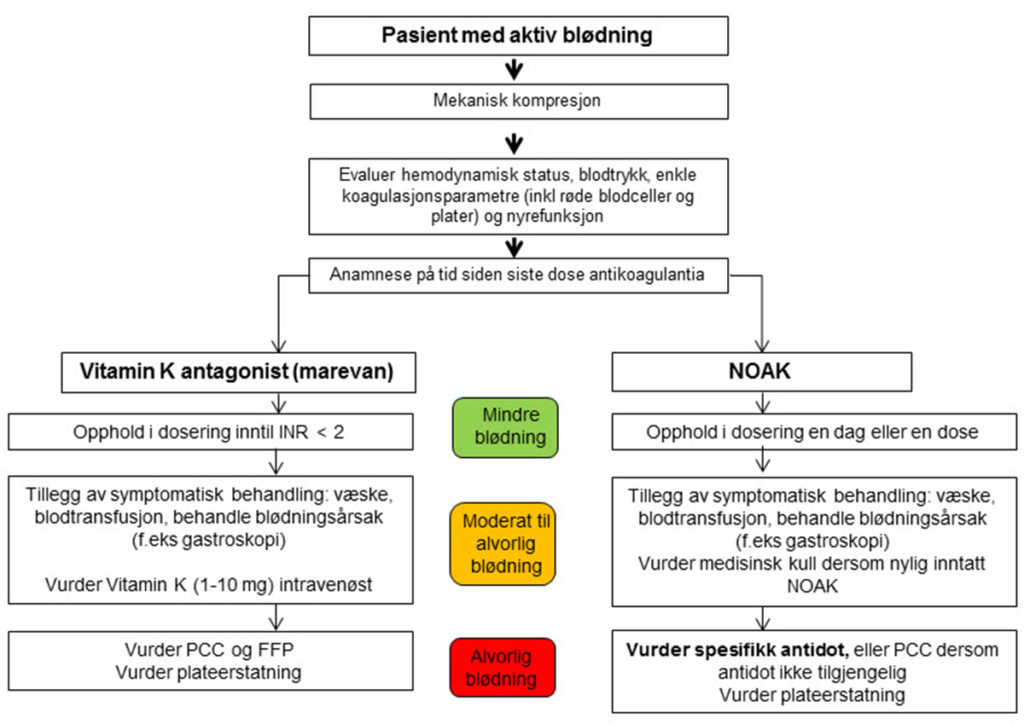
Figur 3. European Society of Cardiology sin anbefalte håndtering av blødning etter alvorlighetsgrad for pasienter på antikoagulasjonsbehandling (10).
Kasuistikken beskriver en 96 år gammel kvinne med permanent AF med CHA2DS 2–VASc skår på 3, som ble hospitalisert med 9-dagers sykehistorie med rektalblødning (16). Hun hadde vært mangeårig behandlet med dabigatran 110 mg x 2. Ved hospitalisering var pasienten ved full bevissthet, men var anemisk med hemoglobin 9,8 g/dL og hadde tegn på alvorlig redusert nyrefunksjon med estimert GFR (Cockroft-Gault formel) på 16 mL/min. Aktivert partiell tromboplastintid (aPTT), et kvalitativt mål på den totale aktiviteten av det interne koagulasjons¬systemet, var forhøyet på 59 sekunder (referansenivå 28-41 sek). Etter initial støttende behandling med krystalloider, ble idarusizumab intravenøst administrert kort tid etter innkomst (2,5 g x 2 intravenøst), og øvre endoskopi ble gjennomført uten funn av blødningsfokus. Etter kort tid stoppet blødningen, uten annen intervensjon, og etter 12 timer ble aPTT målt til 26 sek. Kolonoskopi påviste en tumor i rektum som ble vurdert som fokuset for GI blødningen.
Det er begrensede muligheter for umiddelbart å oppheve antikoagulasjonseffekten til de nye orale antikoagulantia. Avhengig av nyrefunksjon, vil det gå mellom ett og fire døgn før effekten av NOAK går ut (17). Kasuistikken illustrerer imidlertid at for ett av de tilgjengelige nye orale antikoagulantia (dabigatran), kan administrasjon av idarusizumab umiddelbart fasilitere normal hemostase til tross for pågående antikoagulasjon. Således, for pasienter som behandles med dabigatran i behov for øyeblikkelig hjelp ved alvorlige eller livstruende blødninger, eller behov for akutt kirurgi, vil hurtig og spesifikk reversering av antikoagulasjon med idarusizumab være et effektivt hjelpemiddel.
Overlege Ole-Christian Rutherford, overlege Waleed Ghanima og overlege/professor Dan Atar har mottatt foredragsstøtte fra Boehringer Ingelheim, produsenten av idarusizumab. PhD Svein Roseth og lege/PhD Odd Erik Johansen er ansatt i medisinsk avdeling i Boehringer Ingelheim.
Referanser
1. Søreide K, Desserud KF. Emergency surgery in the elderly: the balance between function, frailty, fatality and futility. Scand Journal of Trauma, Resucitation and Emergency Medicine 2015; 23:10.
2. Tveit A, Abdelnoor M, Enger S et al. Atrial fibrillation and antithrombotic therapy in a 75-year-old population. Cardiology 2008;109:258-62.
3. Dossett LA, Riesel JN, Griffin MR et al. Prevalence and implications of preinjury warfarin use: an analysis of the National Trauma Databank. Arch Surg 2011; 146:565-70.
4. Steinberg BA, Peterson ED, Kim S et al. Use and Outcomes Associated With Bridging During Anticoagulation Interruptions in Patients With Atrial Fibrillation. Circulation 2015; 131:488-94.
5. Garcia D, Alexander JH, Wallentin, L et al. Management and clinical outcomes in patients treated with apixaban vs warfarin undergoing procedures. Blood 2014; 124:3692-8.
6. Sherwood A, Douketis JD, Patel MR et al. Outcomes of Temporary Interruption of Rivaroxaban Compared With Warfarin in Patients With Nonvalvular Atrial Fibrillation. Circulation 2014; 129:1850–1859.
7. Haeley JS, Eikelboom J, Douketis J et al. Periprocedural Bleeding and Thromboembolic Events With Dabigatran Compared With Warfarin. Circulation 2012; 126:343-8.
8. Connolly SJ, Ezekowitz MD, Yusuf S et al. Dabigatran versus Warfarin in Patients with Atrial Fibrillation. N Engl J Med 2009; 361:1139-51.
9. Hu TY, Vaidya VR and Asirvatham SJ. Reversing anticoagulant effects of novel oral anticoagulants: role of ciraparantag, andexanet alfa, and idarucizumab. Vasc Health Risk Manag. 2016; 12: 35–44.
10. Kirchhof P, Benussi, S Kotecha, D et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur Heart J 2016;37:2893–2962.
11. Chang DN, Dager WE, Chin AI. Removal of dabigatran by hemodialysis. Am J Kidney Dis. 2013;61:487-9.
12. Pollack CV, Reilly PA, Bernstein R et al. Design and rationale for RE-VERSE AD: A phase 3 study of idarucizumab, a specific reversal agent for dabigatran. Thromb Haemost. 2015; 114:198-205.
13. https://nyemetoder.no/nyheter/innforer-legemiddel-mot-blodningerfor å reversere livstruende blødninger eller ved akutt behov for operasjon.
www.ema.europa.eu/docs/no_NO/document_library/EPAR_-_Product_Information/human/003986/WC500197462.pdf
14. Pollack CV, Reilly PA, Eikelboom J et al. Idarucizumab for dabigatran reversal. N Eng J Med 2015;373:511-20.
15. Pollack CV, Reilly PA, Eikelboom J et al. Idarucizumab for Dabigatran Reversal: Updated Results of the RE-VERSE AD Study. Presented on 15 November at the American Heart Association (AHA) Scientific Sessions 2016, New Orleans, Louisiana.
16. Gendron N, Feral-Pierssens AL, Jurcisin I, et al. Real-world use of idarucizumab for dabigatran reversal in three cases of serious bleeding. Clin Case Rep. 2017;5:346-350
17. Heidbuchel H, Verhamme P, Alings M et al. Updated European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist anticoagulants in patients with non-valvular atrial fibrillation. Europace 2015;17:1467-507.