Sepsis er en listruende tilstand som krever rask oppstart med antibiotika. Kombinasjonsbehandling med penicillin og gentamicin er fortsatt førstevalg ved sepsis og mistenkt sepsis i den reviderte antibiotikaretningslinjen. Ved septisk sjokk er piperacillin/tazobaktam førstevalg.
Torgun Wæhre, seksjonsoverlege dr. med. Infeksjonsmedisinsk avdeling, OUS Ullevål
Anbefalingene om antibiotikabehandling ved sepsis har vært diskutert siden publiseringen av forrige versjon av retningslinjen i 2013. Den norske behandlingstradisjonen med smalspektret penicillin og aminoglykosid som standardbehandling har blitt kritisert av enkelte miljøer for å mangle evidens og påføre pasienter fare for nyreskade. Ved denne revisjonen la vi vekt på å sette sammen et bredt fagnettverk av infeksjonsleger, anestesiologer/ intensivleger, mikrobiologer og en farmasøyt med representasjon fra små og store sykehus i alle helseregioner. Som det eneste kapittelet i den reviderte retningslinjen for antibiotika ble hele kapittelet også sendt på ekstern høring, noe som ga mange og grundige innspill fra fagmiljøer rundt om i landet. Til grunn for arbeidet har vi lagt internasjonale retningslinjer med særlig vekt på Surviving Sepsis Campaign (SSC), de nederlandske SWAB guidelines samt svenske og danske retningslinjer (1-5).
Sepsis defineres etter sepsis-3 kriteriene, som betyr livstruende organdysfunksjon forårsaket av en dysregulert vertsrespons på infeksjon, se tabell 1 (6). Mange pasienter vil ved innleggelse ha mistenkt sepsis uten at organsviktkriteriene nødvendigvis er oppfylt. Disse pasientene vil også omfattes av sepsisanbefalingen. Septisk sjokk er en undergruppe med betydelig økt mortalitet karakterisert av vedvarende hypotensjon tross væskebehandling, i praksis med behov for vasopressor.
Septisk sjokk er skilt ut med egen anbefaling, og vi har laget egne anbefalinger for sepsis uten kjent fokus, og sepsis utgående fra urinveier, abdomen og blodbane. Pasienter med mistenkt luftveisfokus har vi lenket til anbefalingene for alvorlig, svært alvorlig eller komplisert pneumoni, henholdsvis samfunnservervet, sykehuservervet og ventilatorassosiert. Anbefaling om puerperal sepsis er forfattet av fagnettverket for gynekologiske infeksjoner, mens sepsis utgående fra hud og bløtvev vil bli revidert samtidig med resten av hud og bløtvevskapittelet senere dette året.
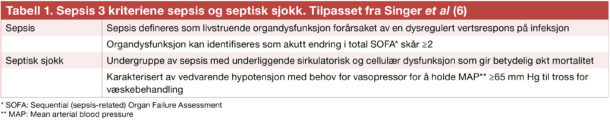
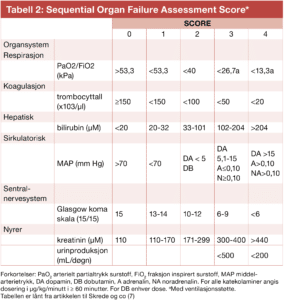
For vurdering av organsvikt ved mistenkt sepsis, anbefales bruk av skåringssystemer i tillegg til klinisk vurdering og utvikling over tid. Bruk av skåringssystemer bør tilpasses lokale forhold ved sykehusene. Sequential Organ Failure Assesment (SOFA) skår er «gullstandarden» for sepsisvurdering, og akutt forverring av SOFA skår≥2 indikerer alvorlig organdysfunksjon, se Faktaboks og Figur (7). National Early Warning Score (NEWS) og quick SOFA (qSOFA) også brukes mye. Alle systemer har sine svakheter som klinikerne må være klar over, særlig har qSOFA lav sensitivitet for å plukke opp pasienter med sepsis. Systemic Inflammatory Response Syndrome (SIRS) kriteriene anbefales ikke lengre.
Hastegrad for antibiotikabehandling ved sepsis har vært et viktig tema i revisjonen. Tidligere norske og internasjonale retningslinjer anbefalte at antibiotika skulle gis innen én time. I Helsetilsynets sepsistilsyn ved norske sykehus (2016-2018) fant man at målet om antibiotikabehandling innen en time ofte ikke ble oppfylt. I den oppdaterte versjonen av Surviving sepsis campaign, som ble publisert høsten 2021, modifiseres denne anbefalingen noe. Man holder fast ved at pasienter med septisk sjokk eller høy sannsynlighet for sepsis bør ha antibiotika innen en time, mens man hos pasienter med mindre mistanke kan gjøre aktiv diagnostikk og observasjon i inntil 3 timer før antibiotikabehandling startes (1). Vi har lagt oss på samme linje i vår anbefaling, og tenker dette gir en mulighet til å skille ut pasientene som ikke har infeksjon (og dermed ikke sepsis) som årsak til alvorlige sykdomstegn, og pasientene som har lokalisert infeksjon uten vesentlig organpåvirkning som kan få mer målrettet antibiotikabehandling.
Antibiotikadoseringene i anbefalingene er basert på doseringsanbefalingene fra The European Committee on Antimicrobial Susceptibility Testing (EUCAST) og den norske Arbeidsgruppen for antibiotikaspørsmål og metoder for resistensbestemmelser (AFA) sitt grunnlag for norsk antibiotikadosering (8). Hos pasienter med septisk sjokk eller alvorlig sirkulasjonspåvirkning gis høyere dosering av de fleste antibiotika, og for betalaktamantibiotikaene anbefales også forlenget infusjon eller hyppigere dosering. Ved forlenget infusjon gis en ladningsdose over kort tid før man begynner med infusjoner som skal gå over 3 timer.
Tabell 2 oppsummerer behandlingsanbefalingene ved sepsis.
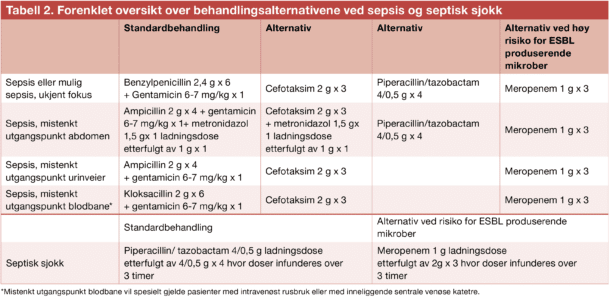
Som sepsisbehandling har kombinasjon av et smalspektret penicillin og et aminoglykosid lang tradisjon i Norge, men dokumentasjonen av effekt og bivirkninger er sparsom. Behandlingen står seg godt med de resistensforholdene vi har i Norge, men gode sammenliknende studier opp mot bredspektrede betalaktamer mangler dessverre. Risikoen for utvikling av akutt nyreskade ved bruk av aminoglykosid hos pasienter med risiko for utvikling av organsvikt har vært et hovedargument mot bruk av disse legemidlene ved sepsis. Disse spørsmålene ble grundig diskutert i fagnettverket og den eksterne høringen. Mange pekte på faren for økt og unødvendig høyt forbruk av bredspektrede betalaktamer hvis aminoglykosidalternativet ble nedtonet. Vi har også innhentet data fra det norske Legemiddelverket som de siste årene har mottatt svært få meldinger om alvorlige bivirkninger av aminoglykosidbehandling. Dette kan tyde på at den bruken vi har hatt av disse legemidlene i Norge har vært trygg.
Konklusjonen er at i de nye anbefalingene vil fortsatt benzylpenicillin+ gentamicin være førstevalg ved sepsis uten kjent fokus uten sjokk. Tilsvarende anbefales ampicillin + gentamicin ved urosepsis, ampicillin + gentamicin + metronidazol ved abdominalsepsis og kloksacillin + gentamicin ved blodbanesepsis. Pasienter med økt risiko for utvikling av akutt nyreskade bør ikke få denne kombinasjonen. Dette gjelder særlig pasienter med kjent kronisk nyresykdom (GFR < 30 ml/min), organtransplanterte, bruk av nyretoksiske medikamenter, ved høy alder og samtidig polyfarmasi, samt ved akutte tilstander som betydelig hypovolemi eller sirkulasjonssvikt. Hos disse pasientene anbefales bredspektrede betalaktamer som tredje generasjons cefalosporiner eller piperacillin-tazobactam. Behandling med karbapenem (meropenem) bør forbeholdes pasienter med høy risiko for infeksjon med ESBL-produserende eller andre multiresistente mikrober. Risiko for sepsis med slike mikrober gjelder spesielt pasienter med kjent kolonisering/ nylig infeksjon med samme mikrober, nylig bredspektret antibiotika eller langvarig sykehusopphold. Lokale resistensforhold og reiseaktivitet kan også vektlegges.
Ved septisk sjokk anbefales piperacillin-tazobaktam, alternativt meropenem ved økt risiko for ESBL eller andre resistente gram-negative bakterier. Begge disse antibiotikaene bør gis i høy dose og med forlenget infusjon ved septisk sjokk. Kombinasjonsbehandling med bredspektret betalaktam + aminoglykosid anbefales ikke, noe som er i tråd med oppdaterte retningslinjer fra Nederland og Surviving sepsis campaign (1, 3).
Et viktig budskap i den nye anbefalingen er at antibiotika må evalueres daglig. Hos mange pasienter kan behandlingen etter 1-2 dager smalnes eller målrettes mot mikrobiologiske funn og infeksjonsfokus. Bruk av aminoglykosid utover 1-2 dager øker faren for toksisitet og bør unngås i de fleste tilfeller. Monitorering med konsentrasjonsbestemmelse er viktig for å redusere risiko for toksisitet, særlig ved behandling utover 2-3 dager. Konferer gjerne med spesialist om antibiotikavalg videre. For betalaktamer kan doser ofte reduseres til standarddoser/ intervaller når det ikke lengre er tegn til påvirkning av sirkulasjon.
Varighet av antibiotikabehandlingen vil avhenge av infeksjonsfokus og mikrobe. For de fleste ukompliserte tilfeller av sepsis utgående fra luftveier, urinveier og abdomen kan man gå over til oral behandling når pasienten er stabilisert og kan spise selv.Total behandlingstid på 7-10 dagers behandling vil ofte være tilstrekkelig, se organkapitlene for nærmere angivelse. Ved bakteremi med gule stafylokokker anbefales alltid minst 14 dagers intravenøs behandling; for dette har vi laget en egen anbefaling i den nye retningslinjen.
1. Evans L, Rhodes A, Alhazzani W, Antonelli M, Coopersmith CM, French C, et al. Surviving sepsis campaign: international guidelines for management of sepsis and septic shock 2021. Intensive Care Med. 2021:1-67.
2. Rhodes A, Evans LE, Alhazzani W, Levy MM, Antonelli M, Ferrer R, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intensive Care Med. 2017;43(3):304-77.
3. SWAB: Stichting Werkgroep Antibioticabeleid. Empirical antibacterial therapy of sepsis in adults. Leiden; 2020.
4. Svenska Infektionsläkarföreningen. Vårdprogram. Sepsis och septisk chock. Østersund: Svenska Infektionsläkarföreningen; 2018.
5. Knudsen J, Boel J, Olsen B, Benfield T, Arpi M, Frimodt-Møller N, et al. Antibiotika – dosering, forholdsregler og behandlingsrekommandationer håndbog. Hovedstadsregionen. København: Region Hovedstaden; 2018.
6. Singer M, Deutschman CS, Seymour CW, Shankar-Hari M, Annane D, Bauer M, et al. The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). Jama. 2016;315(8):801-10.
7. Skrede S, Flaatten HK. Nye internasjonale sepsisdefinisjoner vil påvikre hverdagen vår. Indremedisineren. 2016(02):28-31.
8. The European Committee on Antimicrobial Susceptibility Testing. Dosages (V 10.0) Basel: EUCAST; 2020 [updated 01.01.2020. Available from: https://www.eucast.org/fileadmin/src/media/PDFs/EUCAST_files/Breakpoint_tables/Dosages_v_10.0_Breakpoint_Tables.pdf.