Allogen stamcelletransplantasjon for ALL hos voksne er en effektiv behandling for utvalgte pasienter. I dette materialet så vi på samtlige pasienter som ble behandlet med denne metoden fra 2006-2021. Våre funn viser fallende andel tilbakefall, men en relativt høy behandlingsrelatert mortalitet sammenlignet med internasjonale data.
Torkild Høieggen Pedersen, Lege i spesialisering, avdeling for blodsykdommer Oslo universitetssykehus,
Hilde Skuterud Wik, Overlege PhD, avdeling for blodsykdommer, Oslo universitetssykehus
Tor Henrik Anderson Tvedt, Overlege PhD, avdeling for blodsykdommer, Oslo universitetssykehus,
Akutt lymfoblastisk leukemi (ALL) er en aggressiv kreftform som utgår fra umodne lymfocytter (lymfoblaster). Sykdommen benevnes henholdsvis B- eller T-ALL ettersom kreften utgår fra B- eller T-celler. B-ALL er vanligere enn T-ALL og forekommer hos ca. 70%.
ALL er en av de hyppigste årsakene til kreft hos barn, men regnes som en sjelden sykdom hos voksne med insidens på 0,5-1 per 100 000. Tilstanden utgjør ca. 9% av alle voksne med akutt leukemi.
ALL inndeles i underkategorier basert på genetiske avvik i kreftcellene. Den viktigste gruppen er Philadelphia kromosom positiv ALL som karakteriseres ved translokasjon mellom kromosom 9 og 22. Philadelphia kromosom positiv sykdom forekommer hos ca. 20% av voksne med ALL og er vanligere med økende alder. Sykdomsentiteten kjennetegnes av god respons på kjemoterapi initialt, men svært høy risiko for residiv. Undergruppen skiller seg også fra andre typer ALL ved at målrettet behandling med tyrosinkinasehemmere som imatinib, dasatinib eller nilotinib kan bringe sykdommen i remisjon og kontrollere tilstanden i en periode. Philadelphia kromosom negativ ALL er en heterogen gruppe sykdommer definert av flere forskjellige genetiske avvik. Så langt har man ikke klart å målrette behandlingen mot disse genetiske avvikene.
Den initiale behandlingen av ALL med kjemoterapi kalles induksjonsbehandling. Denne har som mål å redusere andel kreftceller og oppnå regenerasjon av normal benmargsfunksjon. Påfølgende behandling skal forhindre tilbakefall og kurere pasienten. Kurasjon oppnås hos 70-80% av unge voksne, men er betydelig lavere for personer over 65 år. Årsaken til dette er både økt risiko for residiv, men også dårligere toleranse for behandlingen.
Allogen stamcelletransplantasjon er den mest effektive behandlingen for å redusere risiko for tilbakefall, men er beheftet med en ikke ubetydelig risiko for behandlingsrelatert død grunnet toksisitet, infeksjoner og transplantat-mot-vert sykdom (GvHD). I tillegg medfører behandlingen økt risiko for følgetilstander fra de fleste organsystemer, f.eks. svikt i endokrine akser, redusert hjerte- og lungefunksjon og sekundær kreftsykdom. Tverrfaglig oppfølging hos disse pasientene er derfor svært viktig.
Tilstedeværelse av spesifikke genetiske avvik (f.eks. Philadelphia kromosom positiv ALL) og respons på behandlingen er de to viktigste faktorene for å bestemme nytte av transplantasjon. Pasienter som 29 dager etter oppstart av cellegiftbehandlingen har mer enn 5% leukemiske celler i benmargen, eller pasienter som har målbar restsykdom 2-3 måneder etter behandlingsstart ser ut til å ha klar nytte av transplantasjon.
Ved tilbakefall hos voksne som tidligere kun er behandlet med kjemoterapi, kan sykdommen kun kureres med allogen stamcelletransplantasjon. Det er kjent at transplantasjon hos disse pasientene gir økt risiko for alvorlige, potensielt dødelige komplikasjoner. For ALL-pasienter generelt er risiko for tilbakefall svært høy hvis de transplanteres uten reduksjon av tumormasser. Pasientene tilbys derfor først transplantasjon når annen behandling har brakt dem i komplett remisjon. Dette defineres ut fra resterende tumorceller (1-5).
Allogen stamcelletransplantasjon er en viktig tilleggsbehandling av pasienter med ALL som har høy risiko for tilbakefall. Vi har i denne artikkelen utført en retrospektiv analyse av pasienter som ble behandlet med allogen stamcelletransplantasjon ved Oslo universitetssykehus (OUS) som del av primærbehandlingen eller ved tilbakefall. Fokus i analysen er overlevelse, komplikasjoner og risiko for tilbakefall.
Analysen inkluderte alle pasienter som ble behandlet med allogen stamcelletransplantasjon ved avdeling for blodsykdommer, OUS, Rikshospitalet fra 01.01.2006 til 01.05.2021. Målet var å utføre en deskriptiv analyse av indikasjon for transplantasjon, overlevelse, risiko for tilbakefall og komplikasjoner. Behandlingsrelatert mortalitet er definert som død uten påvist tilbakefall. Akutt og kronisk GvHD ble gradert i henhold til standard kriterier (6, 7).
Pasientene ble inndelt i følgende grupper:
Opplysninger er hentet fra avdelingens kvalitetsregister som oppdateres fortløpende. Registeret er godkjent av personvernombudet ved sykehuset og Regionale komiteer for medisinsk og helsefaglig forskningsetikk (#2019/614).
Totaloverlevelse ble estimert ved Kaplan-Meier metoden. Pasientene ble sensurert ved tidspunkt for dødsfall eller ved tidspunkt for datauthenting som var 07.05.21.
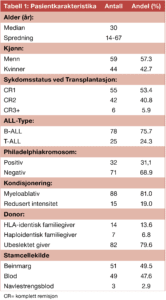
Totalt ble 103 pasienter behandlet med allogen stamcelletransplantasjon, 6 av disse ble transplantert 2 ganger. Pasientkarakteristika er presentert i Tabell 1. 53% av pasientene ble transplantert som del av primærbehandlingen (CR1), mens 41% ble transplantert ved 1. tilbakefall (CR2) og kun 6 pasienter ble transplantert på et senere tidspunkt i sykdomsforløpet (CR3+). Median alder ved transplantasjon var 30 år og noen flere menn enn kvinner ble transplantert. Benmargsutryddende forbehandling (behandling rett før transplantsjonen) ble benyttet hos 81% av pasientene, og 19% mottok forbehandling med redusert intensitet.
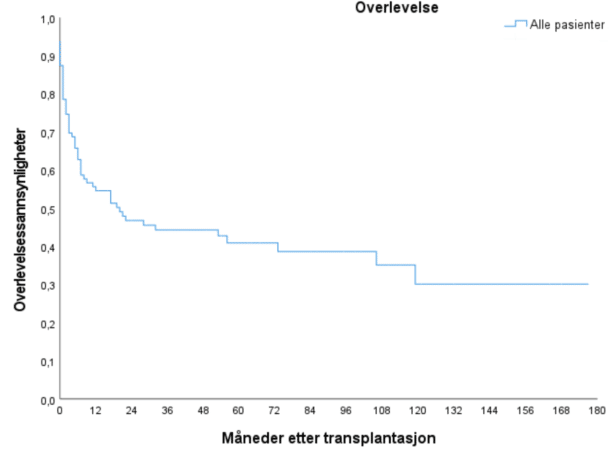
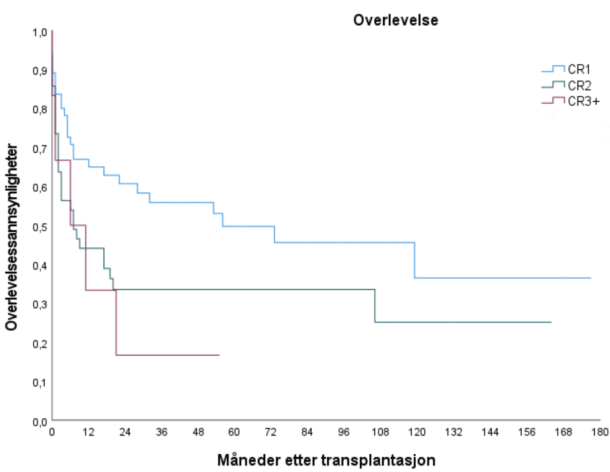
Per 07.05.2021 var 43 pasienter (42%) i live og uten tilbakefall. Medianoverlevelse var 20 måneder etter transplantasjon. 2-års overlevelse var 47%. Pasientene med Philadelphia kromosom positiv (n=32) og Philadelphia kromosom negativ ALL (n=71) hadde median overlevelse på hhv. 106 og 12 måneder og 2-års overlevelse på hhv. 62% og 39%. Pasientene med B- og T-ALL hadde medianoverlevelse på hhv. 32 og 5 måneder og 2-års overlevelse var hhv. 52% og 30%.
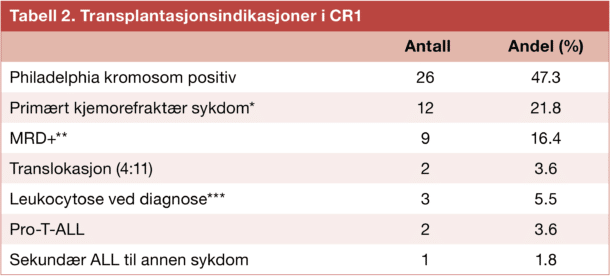
Hensikten med transplantasjon i første remisjon er å forhindre tilbakefall hos pasientene med høy risiko for dette. Årsakene til transplantasjon i CR1 er oppsummert i Tabell 2. Den vanligste indikasjonen for transplantasjon i CR1 var Philadelphia kromosom positiv ALL (47%) etterfulgt av inadekvat respons på kjemoterapi i form av enten betydelig mengde leukemiceller 29 dager etter oppstart behandling eller påvisbare ALL-celler 2-3 måneder etter behandlingsstart (38%).
For pasientene som ble transplantert i første remisjon var medianoverlevelse 56 måneder og 2-årsoverlevelse 61%.
For pasienter med Philadelphia kromosom positiv ALL transplantert i CR1 var 65%. For Philadelphia kromosom negativ ALL var median overlevelse 56 måneder og 2-års overlevelse 56%.
Hovedparten av pasientene som ble transplantert etter tilbakefall hadde Philadelphia kromosom negativ sykdom siden Philadelphia kromosom positiv sykdom i stor grad transplanteres i første remisjon. For pasientene transplantert i CR2 var medianoverlevelsen 7 måneder og 2-års overlevelsen 36%. Medianoverlevelse for pasienter med Philadelphia kromosom positiv ALL (n=6) i CR2 var 3 måneder med 2-års overlevelse på 50%. For Philadelphia kromosom negativ ALL i CR2 var medianoverlevelse 7 måneder og 2-årsoverlelse på 30%. I CR3+ (n=6) hadde alle pasientene Philadelphia kromosom negativ ALL. Medianoverlevelsen var 6 måneder og 2-års overlevelse 17%.
60 pasienter døde i oppfølgingsperioden etter transplantasjon. Behandlingsrelatert død var den vanligste årsaken til dødsfall og inntraff hos 37 av 103 (36%) pasienter (Tabell 3).
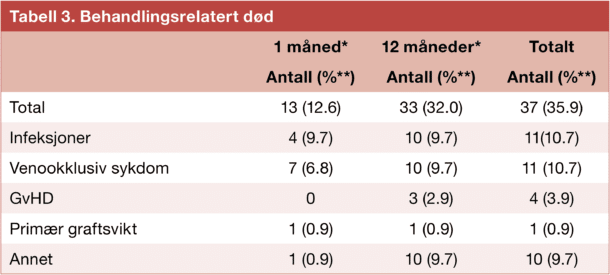
Tilbakefall av ALL var årsak til død hos 20 av 103 (19%) pasienter, halvparten av disse var døde innen 12 måneder etter transplantasjonen. Totalt fikk 27 av 103 (26%) pasienter tilbakefall etter transplantasjon, ved dataanalyse var 4 (15%) av disse fortsatt i live med tilbakefall av ALL ved tidspunkt for sensur.
Hos pasienter som var under 18 år på tidspunkt for transplantasjon (n=11) døde 9 (73%), 3(18%) behandlingsrelatert død og 6 (55%) av tilbakefall. For aldersgruppen 18-45 år (n=71) døde 36 (51%), 24 (34%) av behandlingsrelatert død og 12 (17%) av tilbakefall. For personer over 45 år (n=21) døde 13 (62%). 11 (52% av behandlingsrelatert død og 2 (10%) av tilbakefall.
Akutt GvHD ble observert hos halvparten av pasientene. Imidlertid var de aller fleste forløpene milde og kun 18% utviklet alvorlig akutt GvHD. 14% utviklet mild eller moderat kronisk GvHD, mens 10% utviklet alvorlig kronisk GvHD.
Av de 103 pasientene som ble transplantert ved avdeling for blodsykdommer ved Rikshospitalet i 2006-2021 var median overlevelse 20 måneder med estimert 2-årsoverlevelse på 47%. 36% døde av behandlingsrelaterte årsaker. Som forventet var medianoverlevelsen langt bedre for pasienter transplantert i CR1 sammenlignet med senere remisjoner. Beelen et al. (8) beskriver 542 pasienter med Philadelphia kromosom negativ sykdom transplantert i CR1. Her fant man en estimert 5-års overlevelse på 58% og behandlingsrelatert død på 21%. I en dansk populasjonsbasert studie fra 2022 beskriver Gjærde et al. 181 pasienter som gjennomgikk allogen stamcelletransplantasjon for ALL i perioden 2000-2019 (9). Her fant man 5-års overlevelse på 62% og behandlingsrelatert død på 17%. Begge studiene har bedre resultater enn i vårt materiale både for overlevelse og behandlingsrelatert død.
I historiske data fra vår avdeling (1984-2005) var medianoverlevelsen 18 måneder og leukemifri overlevelse etter fem år 35% (10). Sammenlignet med disse tallene finner vi en økt overlevelse, som drives av færre tilbakefall, men reduseres av økt andel behandlingsrelatert død. Reduksjonen i tilbakefall kan til dels forklares av flere transplanterte i CR1 og strengere kriterier for andel blaster i benmargen før transplantasjon.
Den høye andelen behandlingsrelatert død i vårt materiale synes drevet av toksisitet og infeksjoner i relasjon til kondisjoneringen. Kondisjoneringsregimene som i dag benyttes ved avdeling for blodsykdommer OUS avviker i liten grad fra det som angis i internasjonale publikasjoner og forklarer ikke den reduserte overlevelsen i vårt materiale sammenlignet med disse (9, 11).
Vår kohort på 103 pasienter er liten og resultatene må tolkes med forsiktighet. Særlig subgruppeanalyser blir usikre i en liten pasientpopulasjon. Av den grunn er det ikke gjort analyser over snevrere årsperioder.
Allogen stamcelletransplantasjon er en viktig behandling for pasienter med ALL og høy risiko for tilbakefall, men er forbundet med relativ høy risiko for behandlingsrelatert død, som er noe høyere i vårt materiale sammenliknet med internasjonale data. Både indikasjonene for stamcelletransplantasjon og valg av forbehandling følger internasjonale anbefalinger og vi har ikke funnet en entydig årsak til dette. De senere årene er det gjort kvalitetsforbedrende tiltak som man tror vil føre til bedre resultater. Foreløpig er observasjonstiden for kort til å vurdere effekten av disse tiltakene.