
Bård Waldum-Grevbo
Av Bård Waldum-Grevbo, MD, PhD, Institutt for klinisk medisin, Universitetet i Oslo og Nyremedisinsk avdeling, Oslo Universitetssykehus Ullevål
Flertallet av pasienter med kronisk hjertesvikt har samtidige tegn på kronisk nyresykdom. På tross av dette er nyrepasienter systematisk ekskludert fra studiene som har lagt grunnlag for moderne hjertesviktbehandling. Økt bevissthet hos behandlere, god pasientopplæring og samarbeid mellom kardiologer og nefrologer kan bidra til en bedret håndtering av en sårbar pasientgruppe.
Nyresykdom og hjertesykdom er tett forbundet i det kardiorenale syndrom. Sykdom i det ene organsystemet påvirker funksjon, og kan initiere sykdomsprosesser i det andre. Hver fjerde pasient som hospitaliseres med forverring av hjertesvikt, opplever fall i glomerulær filtrasjonsrate (GFR) under oppholdet. Forverring av nyrefunksjonen er i slike tilfeller en sterk uavhengig prediktor for in-hospital og 1 års mortalitet (1). Ved kronisk hjertesvikt har de fleste pasientene samtidig nyresykdom (2) (Tabell 1). Både redusert glomerulær filtrasjonsrate (GFR) og unormal albuminutskillelse i urinen er sterke prognostiske markører i denne pasientgruppen
(3, 4). På tross av at organsystemene er så tett knyttet sammen har nyrepasienter systematisk blitt ekskludert fra de store studiene som har lagt grunnlaget for moderne hjertesviktbehandling. Tilgjengelige data indikerer at pasienter med redusert nyrefunksjon har samme relative risikoreduksjon av etablert hjertesviktbehandling som nyrefriske. Likevel, er behandlingsnihilisme på grunn av mangel på evidens og frykt for å påføre pasienten ytterligere nyrefunksjonsnedsettelse og andre uheldige effekter av behandling, være medvirkende til den høye sykelighet og dødelighet hos kardiorenale pasienter.
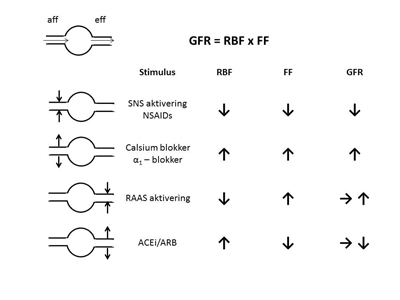
Figur 1: GFR er et produkt av renal blodgjennomstrømming (RBF) og filtrasjonsfraksjon (FF) i glomeruli. Ulike stimuli regulerer vasomotorisk tonus i afferent (aff) og efferent (eff) arteriole og påvirker RBF og FF, og som en konsekvens GFR. Forklaringer på forkortelser brukt i figuren: NSAIDs: non-steroide antiin-flammatoriske medikamenter, Ca blokker: calcium blokker, α1 blokker: alfa-1 symatikoadrenerg blokker, RAAS: renin-angiotensin-aldosteron systemet, ACEi: ACE hemmer, ARB: AII blokker.
GFR er et produkt av renal blodgjennomstrømming og filtrasjonsfraksjonen i glomeruli. Filtrasjonsfraksjonen bestemmes av det intraglomerulære trykket og påvirkes av endret tonus i den afferente (tilførende) og efferente (fraførende) arteriole. Sammen med retensjon av salt og vann, er nevroendokrin aktivering en sentral mekanisme ved hjertesvikt og innebærer aktivering av det sympatiske nervesystemet (SNS) og renin-angiotensin-aldosterion systemet (RAAS) som de viktigste. Begge systemene virker som potente vasokonstriktorer i nyren: SNS virker vasokonstringerende hovedsaklig på den afferente arteriole, mens antiotensin-II virker konstringerende på den efferente arteriole (Figur 1). Resultatet vil være dramatisk redusert renal blodgjennomstrømming ved alvorlig hjertesvikt. Redusert renal blodgjennomstrømming, sammen med økt venetrykk på grunn av væskeretensjon, er ansett som de viktigste utløsende faktorene til en ugunstig cytokinrespons og hypoksisk tubulær skade, og som fører til progredierende tap av nyrefunksjon både ved akutt og kronisk hjertesvikt (5).
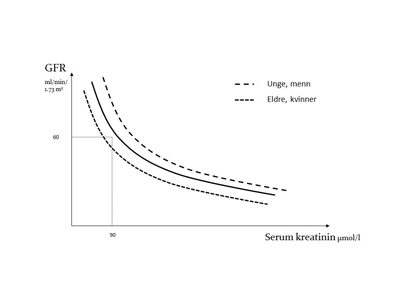
Figur 2: Forholdet mellom serum kreatinin og glomerulær filtrasjonsrate (GFR) er ikke lineært og er avhengig av muskelmasse. Hjertesviktpasienter som ofte har liten muskelmasse, kan derfor ha betydelig redusert nyrefunksjon allerede når serum kreatinin er innenfor laboratoriets referanseområde.
GFR brukes som mål for nyrefunksjon. GFR kan ikke måles direkte, vi er avhengig av å kunne estimere GFR ved å måle nivået av markører som samvarierer med GFR. Serum-kreatinin har lenge vært brukt som markør for nyrefunksjon. Kreatinin produseres i en fast rate av muskelceller, filtreres fritt i glomeruli og sekreres til en viss grad i tubulisystemet. Stigende kreatinin er derfor et resultat av fallende GFR, men stigningen er ikke lineær i forhold til GFR (Figur 2). Serum kreatinin vil i tillegg være avhengig av muskelmasse. Siden de fleste pasienter med hjertesvikt er eldre og har lav muskelmasse, vil GFR ofte allerede være mer enn halvert på det tidspunktet nivået stiger over referanseverdien. Serum kreatinin er derfor en lite sensitiv markør for nyresykdom hos hjertesviktpasienter. Utarbeidelsen av formler for å estimere GFR ut fra serummarkører som kreatinin, hvor man tar hensyn til etnisitet, kjønn og alder, har bidratt til en bedre kategorisiering av nyrefunksjonen. Forbedringer av formlene gjør at vi stadig får bedre anslag for GFR nivå selv i de nær normale områdene. Utover estimert GFR er albu-minutskillelse i urinen den viktigste markøren for å påvise nyresykdom hos hjertesviktpasienter. En forøket albuminutskillelse i urinen undersøkes enklest og best med albumin/kreatinin ratio i spoturin, helst morgenurin. Persisterende forhøyet albuminutskillelse i urinen er en tidlig markør på nyreskade; også ved hjertesvikt, og en sterk prediktor for død; uavhengig av GFR (6).
Pasienter med moderat og alvorlig redusert nyrefunksjon (GFR < 30-45 ml/min/1,73 m2) har systematisk blitt ekskludert fra studiene som har lagt grunnlaget for moderne hjertesviktbehandling. Man mangler derfor i stor grad evidens for hvordan hjertesviktpasienter med samtidig redusert nyrefunksjon best skal behandles. Selv om substudier har vist at pasienter med moderat redusert nyrefunksjon har minst like god effekt av β-blokkere, hemmere av renin-angiotensin systemet og mineralkortikoide reseptoragonister, som de som har normal nyrefunksjon, har hjertesviktpasienter med redusert nyrefunksjon mindre sannsynlighet for å få slik behandling (2). Behandlingsnihilisme er en sannsynlig medvirkende årsak til den dårlige
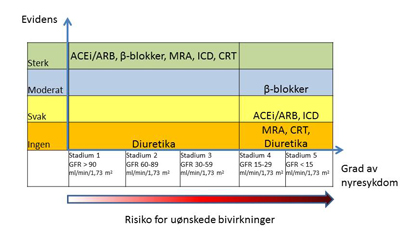
Figur 3. Evidensgrunnlag for effekt av etablert hjertesviktbehandling på dødelighet i forhold til stadier av kronisk nyresykdom. Anbefalt hjertesviktbehandling har god dokumentasjon på effekt også hos pasienter med nyresykdom og GFR over 30 ml/min/1,73 m2. Ved GFR lavere enn 30 ml/min/1,73 m2 er det mangel på studier, men ingen data som tyder på dårligere effekt av behandling. Risiko for uønskede bivirkninger øker derimot med fallende GFR og dette fordrer tettere oppfølging og god pasientopplæring (2).
Figur 2 oppsummerer evidensgrunnlaget for moderne hjertesviktbehandling i lys av pasientens nyrefunksjon. Forenklet kan dataene oppsummeres med at all hjertesviktbehandling som er dokumentert hos nyrefriske, ser ut til å gi tilsvarende relativ risikoreduksjon hos de med moderat redusert nyrefunksjon. I og med at nyresyke har en høyere absolutt risiko for død, kan denne pasientgruppen profittere ekstra godt av anbefalt behandling. Risikoen for uønskede bivirkninger og dekompensert nyresvikt øker imidlertid dramatisk ved fallende GFR og disse pasientene må følges opp ekstra nøye. Svært få studier er gjort på pasienter med GFR under 30 ml/min/1,73 m2, evidensgrunnlaget hos disse pasientene er derfor svært sparsomt. Dette tilsier imidlertid ikke at pasientene ikke har nytte av behandlingen.
Mange medikamenter er avhengige av renal utskillelse. Dosereduksjon i forhold til GFR er derfor anbefalt ved flere medikamenter, inkludert ACE-hemmere. Renal utskillelse av medikamenter er derimot ikke kun bestemt av GFR. Endret tubulær sekresjon og reabsorpsjon av medikamenter og metabolitter som følge av tubulære forstyrrelser reflekteres ikke nødvendigvis av GFR. I tillegg kan nyresykdom påvirke absorpsjon, distribusjonsvolum og proteinbinding av medikamenter på grunn av forstyrrelser i væskebalanse og syre-base balanse (7). Å tilstrebe tradisjonelt anbefalte måldoser er derfor ikke alltid realistisk hos kardiorenale pasienter. Optimal dose hos pasienter med nyresykdom skal derfor defineres individuelt som den til enhver tid høyeste tolererte dose.
Kardiorenale pasienter med kombinert hjertesvikt og nyresykdom balanserer på en smal egg, hvor stimuli som for andre pasienter er ufarlige, kan true balansen mellom adekvat organ perfusjon og organ stuvning. Å balansere den kardiorenale pasienten i det daglige krever en dynamisk tett oppfølging og god pasientopplæring. Man skal tilstrebe adekvate doser av dokumenterte hjertesviktmedisiner, samtidig må man sikre god nyregjennomblødning og opprett-holdelse av GFR. Pasienten må selv ha kunnskap om at varmt vær, febersykdom, lite væskeinntak eller diareepisoder gir risiko for et fall i nyregjennomblødning og forverring av nyrefunksjonen. Risikoen øker med økende alder og alvorlighet av hjertesvikt. Pasienten bør i en slik situasjon selv kunne vurdere reduksjon av diuretika, halvering eller midlertidig å slutte med RAAS- hemmende medisiner. Pasientene må også forstå behovet for en rask blodprøvekontroll i etterkant av slike hendelser. Pasientens behandler må samtidig ha etablert beredskap for å kunne ta imot pasientens henvendelse på kort varsel for å vurdere dynamiske endringer i medikasjon for å bevare pasientens likevekt. Bruk av potente medisiner til en slik sårbar populasjon uten adekvate rutiner for å kontrollere at pasienten tolererer behandlingen, vil kunne føre til alvorlige dekompenseringer. Konsekvensen kan bli at pasient-ene blir fratatt mulighet til potensielt livsviktig behandling
B-type natriuretisk peptid (BNP) og avspaltingsproduktet fra pro-hormonet, N-terminal Pro BNP (NT-ProBNP), er viktige biomarkører for å diagnostisere og monitorere pasienter med hjertesvikt. Epidemi-ologiske studier viste tidlig at pasienter med redusert nyrefunksjon hadde forhøyede verdier av BNP/NT-ProBNP uten objektive tegn til kardiovaskulær sykdom (8, 9). BNP/NT-ProBNP elimineres delvis i nyrene, og oppfatningen blant både kardiologer og nefrologer har vært at forhøyede verdier av biomarkørene hos pasienter med nyresykdom,
er et resultat av akkumulering. På den annen side opptrer økt risiko for kardiovaskulær sykdom tidlig i utviklingen av kronisk nyresykdom (10). Vaskulære endringer med økt karstivhet (11) og tegn til myokarddysfunksjon og inter-stitiell fibrose (12) er påvist hos nyrepasienter selv i tidlige stadier (GFR < 50 ml/min/1,73 m2). Forhøyede nivåer av BNP/NT-ProBNP, og Troponin-T, hos pasienter med nyresykdom kan derfor gjenspeile subkliniske kardiale forandringer, og ikke entydig reflekterer akkumulering. I den norske hjertesviktpopulasjonen fant vi at høye nivåer av BNP/NT-ProBNP predikerte 2-års overlevelse, uavhengig av nyrefunksjonen (13). Vi konkluderte med at BNP/NT-ProBNP reflekterer kardiovaskulær status på prøvetakingstidspunktet uavhengig av nyrefunksjon, og at prøven gir viktig informasjon sammen med GFR nivå, som en prognostisk markør hos hjertesviktpasienter.
Samtidig nyresykdom er svært vanlig hos pasienter med hjertesvikt. Redusert nyrefunksjon er en viktig prognostisk faktor hos disse pasientene. Manglende evidens og frykt for å forverre nyresykdommen ytterligere, bidrar til at pasienter med hjertesvikt og samtidig nyresvikt i mindre grad blir tilbudt dokumentert hjertesviktbehandling. Dette er sannsynligvis medvirkende til pasientgruppens dårlige prognose. Økt bevissthet hos behandlere, god pasientopplæring og samarbeid mellom kardiologer og nefrologer kan bidra til en bedret håndtering av en sårbar pasientgruppe.
Referanser