Pasienter med utbredt kreft er sårbare for en rekke potensielt svært alvorlige komplikasjoner. Disse kan oppstå sekundært til kreftsykdommen i seg selv eller til kreftbehandlingen. Mange av tilstandene er vanlige i akuttmottaket (for eksempel infeksjoner og elektrolyttforstyrrelser) og håndteres antakelig bedre av indremedisinere enn av onkologer. Samtidig er det noen tilstander som er mer spesifikke for onkologien og sjeldnere forekommende. I disse tilfellene kan tiden være knapp og pasientene bør raskt komme til en onkologisk avdeling.
Kathrine F. Vandraas, spesialist i onkologi og overlege ved seksjon for brystonkologi, avdeling for Kreftbehandling, Oslo Universitetssykehus, Radiumhospitalet
Forekomsten av kreft er økende, og om lag 100 personer får diagnosen hver dag. Tre av fire vil bli langtidsoverlevere (i live ≥ 5 år etter diagnose) og for noen kreftformer er overlevelsen tett på 100%. Blant pasienter som ikke blir kurert, lever stadig flere lengre med kreft, og mottar ulike former for systemisk kreftbehandling. Med immunterapiens inntog, ser vi nå undergrupper av pasienter med langvarige remisjoner (flere år). Indikasjoner for bruk av immunterapi og annen målrettet behandling øker stadig. Det er ikke lenger et likhetstegn mellom kreft med spredning og kort forventet levetid, og det legger føringer for «satsningsnivået» når disse pasientene får alvorlige komplikasjoner.
Både kreftsykdommen i seg selv og kreftbehandlingen gir økt risiko for komplikasjoner. Dette er pasienter som ofte har nedsatt reservekapasitet og organdysfunksjon, noe som gjør dem særlig sårbare for et alvorlig forløp. Primærsvulsten eller metastasene kan invadere kritiske strukturer (sentrale blodkar, CNS, luftveier, hjertet) og forårsake kompresjon, trombose, økt trykk eller blødning. Kreftbehandlingen i seg selv kan gi immunsvikt, tumorlyse, autoimmunitet og benmargs- og nyresvikt, for å nevne noe. Når en pasient med utbredt kreftsykdom oppsøker akuttmottaket med nyoppståtte symptomer bør de vurderes raskt med henblikk på noen få akutte onkologiske tilstander der tiden kan være knapp og prognosen avhenger av rask diagnostikk og behandling. I denne oversikten nevnes tre slike tilstander, men listen er ikke uttømmende.
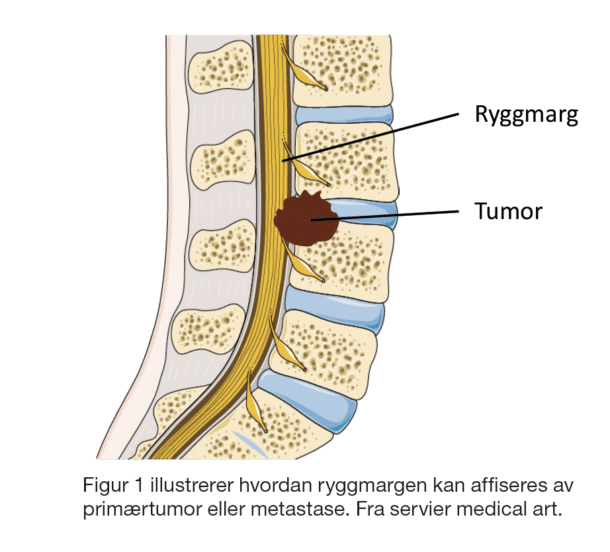
MMK er definert som malign tumorvekst fra corpus vertebrae eller omliggende strukturer med påfølgende trykk mot medulla spinalis. Vanligst lokalisasjon er thorakalcolumna, og prosessen kan medføre små blødninger, inflammasjon og ødem lokalt i området. Dette er en relativt vanlig tilstand hos pasienter med utbredt kreft; 3-5% av pasientgruppen utvikler dette i forløpet. MR er gullstandard for billeddiagnostikk og dette skal tas raskt ved nyoppstått nevrologi hos disse pasientene. Det kliniske bildet vil kunne variere fra kun radiologiske funn og asymptomatisk pasient, til fulminant paraplegi. Symptomene avhenger av affisert nivå i columna: Som regel opplever pasienten først smerter, deretter sensibilitetsutfall og til slutt motorisk affeksjon. Hvis nevrologiske symptomer vedvarer mer enn 72 timer, er det lite sannsynlig at pasienten vil gjenvinne funksjon. Første tiltak er å ringe til vakthavende onkolog ved nærmeste stråle-onkologiske senter. Ved OUS er det utarbeidet standardisert pasientforløp for MMK som ligger tilgjengelig på nett (eHåndbok – Malign medullakompresjon (MMK) – Standardisert pasientforløp (ous-hf.no)) hvor håndtering og oppgavefordeling er detaljert beskrevet. Det understrekes at det er onkolog som har ansvar for å konferere med nevrokirurg. Ved MMK er det indikasjon for steroider (for eksempel deksametason 8 mg x 2 eller 16 mg x 1 / dag) som bør igangsettes umiddelbart etter at man ha konferert med onkolog. Det er sjelden at dette vil forkludre videre diagnostikk og det er viktigere å unngå permanente nevrologiske utfall. De fleste pasienter er ikke kandidater for kirurgi, og skal dermed ha strålebehandling mot affisert område, som regel 10 behandlinger med fotonbestråling (3 Gy x 10 til 30 Gy) som inneliggende pasienter. Unge pasienter med lite tumoraffeksjon (ett nivå), relativt god prognose (> 3 mnd forventet overlevelse) og intakt gangfunksjon kan vurderes for nevrokirurgi.
VCSS er definert som obstruksjon av blodstrømmen gjennom vena cava superior med påfølgende økende trykk i det venøse systemet og dannelse av kollateraler. Symptomer vil avhenge av hvor mye av lumen som er obstruert og hvor raskt tilstanden forverres. Noen pasienter er asymptomatiske, mens andre kan ha hevelse og rødme i ansikt og hals, struttende vener på hals og thorax og i verste fall tungpust, hoste og cyanose som tegn på respirasjonssvikt. Underliggende årsak er som regel malignitet (90%) og da fortrinnsvis fra primær utbredt lungekreft eller lymfom, eller metastaser til intrathorakale lymfeknuter. Tilstanden krever rask diagnostikk og skal utredes med CT thorax og man bør ha tett kommunikasjon med onkolog. Pasientene bør raskt få steroider (for eksempel deksametason 8 mg x 2 eller 16 mg x 1 / dag). Dersom det er mistanke om nyoppstått primært lymfom bør man forsøke å sikre biopsi først, men ved livstruende symptomer skal behandling prioriteres. Noen vil ha behov for intensivbehandling grunnet respirasjonssvikt. Stentinnleggelse vil gi effektiv lindring av plagene for 90% av pasientene, og stråling og eventuelt annen systemisk kreftbehandling er aktuelt etterpå. I nasjonal faglig retningslinje for lungekreft er VCSS omtalt mer detaljert (Vena cava superior syndrom (VCSS) – Stokes krage – Helsedirektoratet
Indikasjonene for bruk av immunterapi øker stadig. Gruppen inkluderer først og fremst sjekkpunkt-hemmere og terapeutiske antistoffer, men også kreftvaksiner og CAR-T-behandling. For noen kreftformer er dette førstevalg i en metastatisk setting (blant annet lunge, malignt melanom, nyre), og prognosen har endret seg dramatisk for undergrupper av pasienter. Behandlingen, som primært er rettet mot T-celle funksjoner i kroppen, medfører også risiko for helt andre bivirkninger enn hva vi ser ved tradisjonell kreftbehandling. Disse kan oppstå når som helst i behandlingsforløpet (også etter seponering), og ramme i prinsippet alle organer i kroppen. Det er særlig kombinasjonsbehandling med monoklonale antistoffer som er forbundet med alvorlig autoimmunitet. Bivirkningene gir ofte inflammasjonsforandringer, antakelig på grunn av celledrapet i seg selv med medfølgende signalstorm i kroppen. Det er viktig for leger i akuttmottak å være oppmerksomme på disse tilstandene.
Immunterapi-relatert toksisitet graderes etter common terminology criteria for adverse events (CTCAE) fra 1-5 , der det vanligste er grad 1-2. Det er først og fremst hud, slimhinner og kjertelvev som rammes. Milde bivirkninger krever ikke seponering av behandlingen, for eksempel kløende dermatitt, akne eller mild diaré. 10% til 30% av pasientene vil oppleve grad 3-4 bivirkninger og 1-2% vil være fatale. CTCAE grad 2 og høyere vil medføre pausering eller seponering av behandlingen og det vil være indikasjon for immundempende behandling. Man bør konferere med onkolog før man igangsetter dette fordi det vil i prinsippet redusere effekten av kreftbehandling.
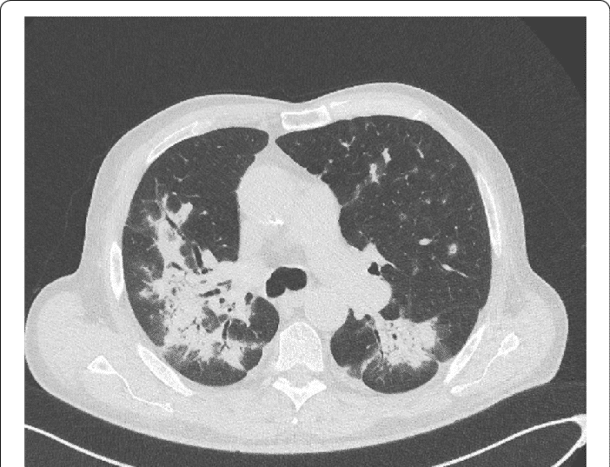
Pneumonitt er den vanligste immunterapi- relaterte bivirkningen i luftveiene og karakteriseres av tungpust, irritasjonshoste og redusert allmenntilstand. Noen pasienter har feber. CT thorax vil kunne avdekke potensielt utbredte, heterogene forandringer forenelig med medikamentutløst inflammasjon. Tilstanden er sjeldnere enn forandringer i hud og slimhinner, men nevnes fordi det kan utvikle seg til lungesvikt og være dødelig. BAL bør utføres og pasienten trenger ofte høye doser steroider.
Det er steroider som er hjørnestenen i behandlingen av immunterapirelatert toksisitet når symptomene tilsier dette. Ofte må man opp i doser rundt 2-4 mg/kg kroppsvekt/per døgn. Fordi steroider også rammer T-celler involvert i eliminasjon av kreftceller, skal man raskt trappe dette ned når pasienten er bedre. Symptomer som er steroidresistente kan behandles med tillegg av andre immunsuppressiva som TNF-alfahemmere eller anti-interleukin-6, men da i tett samråd med onkolog. Norsk Legemiddelhåndbok har detaljert omtale av immunterapi relatert toksisitet (T2.1.3 Bivirkninger av immunterapi | Legemiddelhåndboka (legemiddelhandboka.no) og European Society for Medical Oncology (ESMO) har publisert en egen håndbok på temaet (Toxicities from Immunotherapy | ESMO
Moderne kreftbehandling gjør at mange pasienter lever med utbredt kreftsykdom over lang tid. Disse pasientene er av ulike grunner sårbare for alvorlige komplikasjoner, på grunn av sykdommen i seg selv eller behandlingen. Noen av disse komplikasjonene, slik som MMK, VCSS og immunterapi-relatert toksisitet, krever rask onkologisk håndtering, for at utfallet skal bli så godt som mulig. Da er vi avhengig av et god samarbeid på tvers av spesialitet og sykehus. Det er ikke lenger slik at utbredt kreftsykdom i seg selv er ensbetydende med kort forventet levetid, og satsningsnivå for behandling av akutte komplikasjoner må ta høyde for dette. Når det er sagt, så er særlig MMK og VCSS forbundet med alvorlig prognose, og i visse tilfeller vil det være mest riktig å gjøre minst mulig utover optimal symptomlindrende behandling. Fordi bruken av immunterapi og annen målrettet behandling øker, vil pasienter med immunrelatert toksisitet blir vanligere å se i akuttmottaket. Det er vel verdt tiden å gjøre seg kjent med denne formen for kreftbehandling og hvordan bivirkninger kan arte seg og best håndteres.
Kreft i Norge (kreftregisteret.no)
eHåndbok – Malign medullakompresjon (MMK) – Standardisert pasientforløp (ous-hf.no)
Vena cava superior syndrom (VCSS) – Stokes krage – Helsedirektoratet
T2.1.3 Bivirkninger av immunterapi | Legemiddelhåndboka (legemiddelhandboka.no)