De nye fedmemedisinene forskrives nå til store pasientmengder. Det er derfor viktig at både pasient og behandlende lege er godt informert om riktig og trygg bruk av disse medikamentene.
Sindre Lee-Ødegård, MD, Ph.d., lege ved Seksjon for forebyggende kardiologi, Avdeling for endokrinologi, sykelig overvekt og forebyggende medisin, Oslo universitetssykehus, og seniorforsker ved Universitetet i Oslo.
Serena Tonstad, MD, MPH, Ph.d., overlege ved Seksjon for forebyggende kardiologi, Avdeling for endokrinologi, sykelig overvekt og forebyggende medisin, Oslo universitetssykehus og adjunkt professor, Loma Linda University, California.
Andelen nordmenn med overvekt eller fedme er nå høyere enn andelen med normal vekt (1). Behandlingen for overvekt og fedme inkluderer livstils-intervensjon, med et sunt kosthold, økt fysisk aktivitet og fokus på helseatferd, tillegg av støttemedikasjon, og evt. fedmekirurgi. Medisiner som kan brukes i vektreduserende behandling (2) i Norge er per i dag bupropion-naltrekson (Mysimba®) (3), orlistat (Xenical®) (4), og i senere tid også GLP-1-analoger (glucagon-like peptide-1) (5). GLP-1-analogene liraglutid (Saxenda®) og særlig semaglutid (Wegovy®) har nylig fått stor oppmerksomhet (6, 7). I de tre landene (USA, Danmark og Norge), som nylig har innført Wegovy® som behandling mot overvekt/fedme, har antallet forskrivninger økt enormt (8). Wegovy® er den mest effektive medisinen på norsk marked og har sammen med livsstilstiltak resultert i et gjennomsnittlig vekttap på 15% etter 68 uker (9), som også var vedlikeholdt etter ca. to år (10). Det er verdt å nevne at det finnes flere ulike GLP-1-analoger, og de fleste reduserer kroppsvekten (11), men det er kun Saxenda® og Wegovy® som er godkjent for behandling av overvekt/fedme i Norge. Mange leger kommer derfor sannsynligvis til å forskrive disse medisinene, eller må forholde seg til dem i klinisk praksis i tiden som kommer. Denne artikkelen gir en kort introduksjon til GLP-1-analogene, og avsluttes med råd ved forskriving og oppfølging av medisinering.
I 2008 innførte amerikanske FDA (Food and Drug Administration) et krav om sikkerhetsstudier mtp. hjerte- og karsykdom, og død, ved bruk av nye medisiner mot diabetes type 2 (12). Ti år senere viste en studie lavere risiko for hjerte- og karsykdom og lavere dødelighet ved bruk av liraglutid som blodsukker-reduserende preparat (13). En av tilleggseffektene av både liraglutid (13), og semaglutid (14) var vekttap. Allerede i 1987 ble det vist at GLP-1-reseptoren er uttrykt flere steder i hjernen (15). I 1996 ble det vist at GLP-1 har en hemmende effekt på matinntak og kroppsvekt, noe som bidro til hypotesen om at personer med fedmesykdom har en mangelfull GLP-1-respons (16). Liraglutid ble demonstrert å redusere kroppsvekten til forsøksdyr allerede i 2001 (17). Likevel vakte de humane resultatene stor oppmerksomhet (13, 14) og ledet senere til at disse medisinene ble utviklet og godkjent som behandling mot overvekt og fedme i Norge i hhv. 2019 for liraglutid og i 2023 for semaglutid.
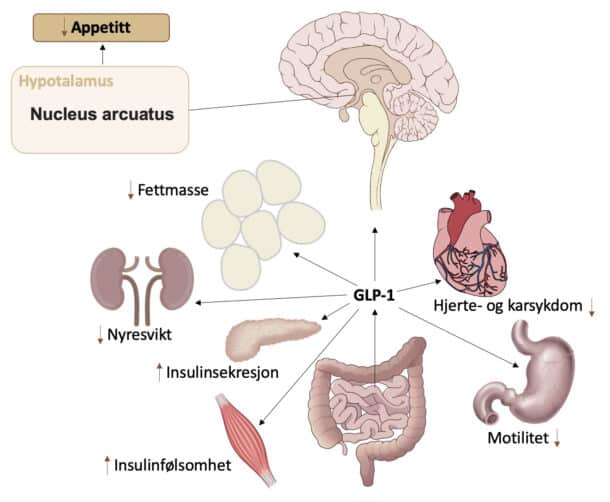
Behandling med GLP-1-analoger leder trolig til vekttap gjennom en kombinasjon av redusert appetitt og lavere energiinntak (18). GLP-1 er et peptid som frigjøres fra L-celler i tarmen som respons på mat i tarmen, og bidrar til en rekke fysiologiske virkninger. GLP-1-analoger er assosiert med mindre sult, preferanse for mindre energitette matvarer, endringer i belønningssystemet for mat og et mer kontrollert spisemønster (18). Dette oppstår trolig ved binding til GLP-1-reseptorer i nucleus arcuatus i hypotalamus (19). Dette området i hypotalamus integrerer sirkulerende signaler for sult og metthet som gjenspeiler kroppens energilagre og tilgjengelighet av næringsstoffer (19). GLP-1-analoger kan også lede til en forsinkelse i gastrisk tømming (20). Farmakologiske studier med GLP-1-analoger har vist forsinket gastrisk tømming den første timen etter matinntak, mens total gastrisk tømming ikke er påvirket (21, 22).
GLP-1-analoger kan gis til voksne med initial kroppsmasseindeks (KMI) ≥30 kg/m2 (fedme), men kan også vurderes for voksne med KMI ≥27-<30 kg/m2 (overvekt) ved forekomst av minst én vektrelatert komorbiditet, slik som dysglykemi (prediabetes eller diabetes mellitus type 2), hypertensjon, dyslipidemi, obstruktiv søvnapné eller hjerte- og karsykdom (23). Liraglutid (Saxenda®) kan vurderes forskrevet til ungdom ≥12 år med fedme (kjønnsspesifikk iso-KMI ≥30) og kroppsvekt >60 kg etter nøye tverrfaglig vurdering, ledet av pediater (24). Vi gjør oppmerksom på at det er særlig personer med sykelig overvekt, dvs. KMI ≥40 eller KMI ≥35-<40 kg/m2 ved forekomst av minst én vektrelatert komorbiditet, som kan ha mest nytte av en GLP-1-analog som hjelp til vektreduksjon.
Det er også viktig at GLP-1-analogene skal brukes samtidig med livsstils-intervensjon i form av forbedret kosthold, økt fysisk aktivitet og helseatferdstiltak (2, 9, 25). Pasientene bør få kostholdsveiledning og starte med fysisk aktivitet, i tråd med nasjonale anbefalinger (23, 26). Helsefremmende kosthold og regelmessig fysisk aktivitet er viktig for å oppnå tap av fettmasse og vedlikehold/økning av muskelmasse (25), men pasientene bør vite at det har mange andre gunstige helseeffekter, uavhengig av effekter på kroppsvekt.
Den mest aktuelle GLP-1-analogen mot overvekt og fedme er Wegovy®. Wegovy® doseres én gang i uken, på fast ukedag, og trappes opp trinnvis. Startdosen er på 0.25 mg og doseres hver uke i fire uker. Deretter trappes dosen opp hver fjerde uke til 0.5 mg, 1.0 mg, 1.7 mg og tilslutt 2.4 mg, som er vedlikeholdsdosen. Ozempic®, som er en medisin mot diabetes type 2, trappes opp på samme måte som Wegovy®, men vedlikeholdsdosen av Ozempic® er 1.0 mg per uke. Hvis pasienten har dysregulert diabetes type 2, kan det foreligge indikasjon for økning av Ozempic®-dosen opp til 2 mg per uke. Saxenda® doseres daglig og trappes opp i intervaller på én uke. Startdosen med Saxenda® er 0.6 mg, som økes til 1,2 mg, 1,8 mg, 2.4 mg og 3.0 mg, som er vedlikeholdsdosen.
Pasienter som selv har, eller har noen i familien med medullært tyroidea karsinom, pasienter med «multiple endocrine neoplasia syndrome type 2» (MEN2), eller pasienter som har kjent overfølsomhet for virke- eller innholdsstoffer i medisinen, skal ikke bruke GLP-1-analoger (27, 28).
Basert på data fra dyr og gnagere (28) frarådes gravide og ammende å bruke GLP-1-analoger. Bekymringen retter seg spesielt mot potensiell risiko for underernæring hos foster/barn. Både hos menn og kvinner bør GLP-1-analoger avsluttes 6-8 uker før planlagt graviditet for at blodkonsentrasjonen av virkestoffet skal bli tilstrekkelig lavt (28). GLP-1-analoger anbefales heller ikke ved amming, med mindre kvinnens helse av ekstraordinære årsaker er mer tjent med effekten av GLP-1-analogen enn risikoen for påvirkningen av barnet (sjeldent aktuelt scenario).
Utvikling av tyroid c-celle tumor (medullært tyroidea karsinom) er en svært sjelden, men en potensielt alvorlig risiko ved bruk av GLP-1-analoger (27). Legen bør se etter symptomer og tegn på tyroidea-tumor, slik som oppfyllinger i hals/nakke-området, dysfagi, tungpust eller heshet.
Gallesten og kolecystitt forekommer ved raskt og kraftig vekttap, og ses også med GLP-1-analog (28). Utredning og behandling er indisert. GLP-1-analogen kan seponeres til gallesykdommen er avklart, og kan deretter startes opp igjen når klinikken tilsier dette.
GLP-1-analoger kan i sjeldne tilfeller gi pankreatitt (28). Mild akutt pankreatitt oppstod i STEP1-studien (9) hos tre pasienter (0.2%) i intervensjonsgruppen mot ingen i placebogruppen. Det finnes lite data på GLP-1-analog-behandling hos pasienter som har gjennomgått pankreatitt tidligere (28). Unngå oppstart av GLP-1-analog ved akutt pankreatitt, gjennomgått pankreatitt siste 6-12 mnd., kronisk pankreatitt eller ved pankreatitter som fluktuerer (28). Hvis en GLP-1-analog startes på en pasient som har gjennomgått en pankreatitt fra mer enn 6-12 mnd. siden, anbefales forlenget opptrappingsperiode, for eksempel to mnd. per dosetrinn. Pasienten må informeres om pankreatittsymptomer og seponering av medisinen hvis disse oppstår. Hos denne pasientgruppen må man vurdere å følge amylase/lipase-konsentrasjon i blodet jevnlig, for eksempel før hver doseøkning .
Hypoglykemi oppstår som hovedregel hos pasienter som behandles med insulin eller sulfonylureaderivater (28). GLP-1-analoger kan forsterke dette, og en tommelfingerregel er å redusere dosen insulin eller sulfonylurea med 20%-30% ved oppstart.
Allergiske reaksjoner kan alltid forekomme. De vanligste er lokale reaksjoner ved innstikkstedet. Det anbefales å variere innstikkstedet (mage, overarm og lår). Foruten antihistaminer, kan man kan evt. forsøke steroider lokalt (for eksempel Dymista® nesespray på huden, men vær oppmerksom, det er utenom indikasjonsområde). Alvorlige reaksjoner/anafylaksi er sjeldne, og GLP-1-analogen seponeres og pasienten må innlegges på sykehus som øyeblikkelig hjelp.
Hos pasienter med diabetes kan en evt. diabetesretinopati forverres ved oppstart av behandling med en GLP-1-analog med et raskt fall i blodglukose-nivået (29). Henvisning til øyelege ved oppstart av en GLP-1-analog bør vurderes for pasienter med diabetes, særlig ved kjent alvorlig retinopati.
Takykardi er en bivirkning av GLP-1-analogene, men mekanismen er ukjent. Det er derfor fornuftig å måle pulsen jevnlig, i alle fall før og etter oppstart behandling. Ved markant pulsøkning som f.eks. hvilepuls >100 eller ved symptomer på takykardi, bør dose GLP-1-analog reduseres eller evt. seponeres.
Akutt nyresvikt kan oppstå ved bruk av GLP-1-analoger, og er som regel en pre-renal svikt pga. dehydrering. Det er generelt viktig å informere pasientene om tilstrekkelig vanninntak når matinntaket reduseres, for eksempel ca. 1.5-2 L vann om dagen. Det er også viktig å måle eGFR før oppstart (30). eGFR<30 bør anses som en kontraindikasjon mot oppstart av GLP-1-analoger. Det er fornuftig å måle eGFR regelmessig, særlig hvis pasienten hadde redusert eGFR før oppstart.
Uventet stor vektreduksjon kan i sjeldne tilfeller være tegn på underliggende malign sykdom, og det er viktig at behandlende lege er oppmerksom på nyoppståtte symptomer eller tegn hos denne pasientgruppen.
Leger må på generell basis være oppmerksomme på depressive symptomer og selvmordstanker hos pasienter som skal starte med vektreduksjon. Fedmemedikamenter, inkl. GLP-1-analoger, bør avventes hos denne pasientgruppen inntil de er stabilisert, og bør avsluttes hos pasienter som får depressive symptomer eller selvmordstanker etter oppstart.
Pasienter med tidligere gastroparese, hjertesvikt NYHA klasse 4, inflammatorisk tarmsykdom eller diabetes type 1 bør i utgangspunktet ikke starte med en GLP-1-analog (28). Hos personer med diabetes type 1 kan denne behandlingen vurderes hvis vekttap er særlig ønskelig, men man bør da informere pasienten godt om symptomer på utvikling av diabetisk ketoacidose (31).
Kombinasjonsbehandling. Pasienten som behandles med en annen GLP-1-analog eller en dipeptidylpeptidase-4 (DDP4)-hemmer (som har en lignende mekanisme (32)), eller bruker annet vekttapsmiddel slik som Mysimba®, bør i utgangspunktet beholde nåværende medisin, eller bytte til kun Wegovy®, evt. Saxenda®. Legen kan vurdere å kombinere flere medikamenter mot fedme, men kunnskapsgrunnlaget på dette er svakt, og pasienten bør følges opp tett for uønskede bivirkninger/hendelser.
Ved oppstart av behandling anbefales det å måle blodkonsentrasjonene av hemoglobin, Na, K, transaminaser, TSH, kreatinin, eGFR, total-, lipider (total-, LDL- og HDL-kolesterol og triglyserider), glukose (fastende) og HbA1C. Ved kjent diabetes type 2 og spørsmål om manglende egenproduksjon av insulin bør fastende c-peptid måles (husk samtidig glukose), og ved tidligere pankreatitt kan amylase eller lipase overveies. Disse nevnte prøvene er viktige for å oppdage udiagnostisert nyresvikt, hypotyreose, leversvikt og diabetes; tilstander som kan kreve forbehold ved behandling.
Pasienten forklares at GLP-1-analogene skal kun brukes sammen livsstilstiltak (kosthold, fysisk aktivitet og helseatferd), og at virkningsmekanismen til GLP-1-analogene kan sammenlignes med et metthetshormon: jo høyere konsentrasjon, dess raskere metthetsfølelse og lavere matinntak (5). De vanlige bivirkningene er kvalme, forstoppelse, løs avføring, hodepine, slapphet og lette øvre mageplager. Hvis disse er veldig uttalte og vedvarer over tid (se under for detaljer ang. bivirkninger), bør lege kontaktes (28). Nedsatt appetitt er forventet og adekvat hydrering er viktig. Det er viktig å fortelle pasientene om risikoen for dehydrering, spesielt ved opphold i varme strøk og på varme sommerdager, eller hvis de også bruker en natriumglukose-kotransportør 2 (SGLT2)-hemmer (ofte relevant for pasienter med diabetes type 2).
De vanligste bivirkninger har sammenheng med effekten GLP-1 har på gastro-intestinaltractus. Vektnedgang er også assosiert med lavere blodtrykk, som sammen med lavt væskeinntak kan påvirke cerebral blodstrøm og relaterte symptomer. Tabell 1 illustrerer de vanligste bivirkningene av GLP-1-analoger og forslag til hvordan disse kan håndteres basert på klinisk erfaring.
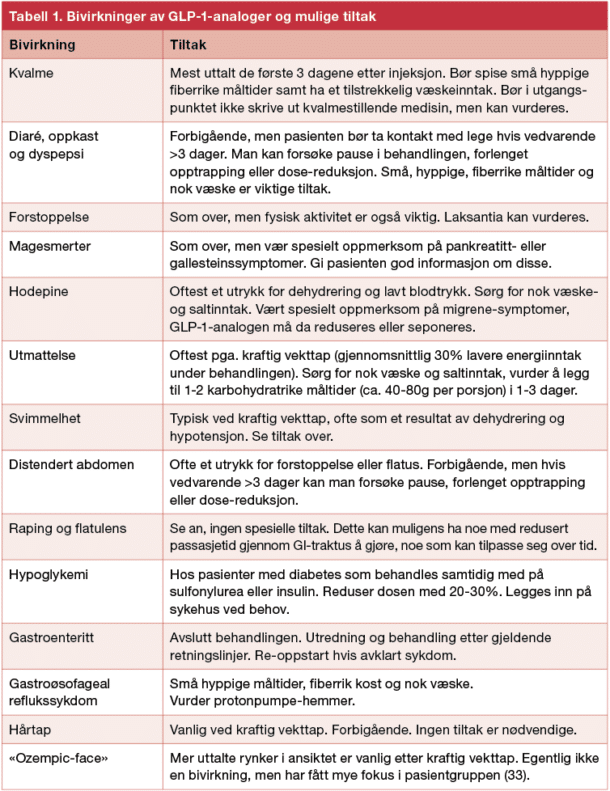
Dosejusteringer kan være nødvendige for å redusere bivirkninger. Dette kan gjøres ved å avstå fra en eller flere doser frem til bivirkningene gir seg, eller forlenge doseintervallet fra syv til ti dager i en periode. Selv om standard opptrappingsregime er fire uker per dosetrinn, kan man ofte bruke lengre tid på hvert dosetrinn for å unngå bivirkninger. I praksis kan man ofte benytte lavere vedlikeholdsdose enn anbefalt (semaglutid 2.4 mg), all den tid pasienten har effekt av medisinen. Hvis pasienten opplever bivirkninger ved doseøkning til neste trinn, reduseres dosen en periode, men forsøkes doseøkning minst én gang til ved et senere tidspunkt, slik det ble gjort i STEP1-studien (9). Hvis pasienten likevel ikke tolererer 2.4 mg semaglutid per uke, kan høyeste tolererte dose benyttes. Noen pasienter opplever effekt på doser så lave som 0.25-0.5 mg ukentlig, og mange har god effekt av 1 mg ukentlig.
I STEP1-studien oppnådde deltagerne et gjennomsnittlig vekttap på ca. 15% etter ett år (9), som også var vedlikeholdt ved oppfølging etter ca. 2 år ved fortsatt bruk av høyeste tolererte dose semaglutid (2.4 mg per uke for de fleste) (10). Ved seponering av semaglutid vil derimot de fleste oppleve økt sultfølelse og vektøkning opp mot utgangsvekten (34). Fedme er for mange en kronisk sykdom med vedvarende forstyrrelser i mekanismene som kontrollerer kroppsvekten. Behandlingen med GLP-1-analoger kan ikke fjerne underliggende årsaker og er kun virksom så lenge den kontinueres. Dette tyder på at man må fortsette å bruke en GLP-1-analog så lenge man har som mål å vedlikeholde oppnådd vekttap. Effekten av kronisk bruk av GLP-1-analoger virker trygg, bl.a. basert på 2-års data i en populasjon med overvekt/fedme uten diabetes type 2 (10) og 2.1-års (14) og 3.8-års (13) data fra pasienter med diabetes type 2.
En legekonsultasjon bør finne sted før oppstart med en GLP-1-analog, og pasientene bør tilbys jevnlig legeoppfølging, for eksempel hver 3. – 6. mnd., med mulighet for tidligere kontakt ved nyoppståtte symptomer. Hvis en pasient enten ikke tolererer behandlingen eller ikke har noen effekt av GLP-1-analogen, bør denne seponeres. Pasienten kan vurderes henvist til fedmekirurgi hvis det foreligger indikasjon for dette.
De nye GLP-1-analogene kan nå forskrives til store pasientmasser. Det er derfor viktig at leger er oppmerksomme på trygg bruk, optimale livsstilstiltak og tett/regelmessig oppfølging av pasienter som benytter seg av denne behandlingen.
Sindre Lee-Ødegård har ingen interessekonflikter.
Serena Tonstad har mottatt honorar for foredrag fra produsenter av vektreduserende medisiner (Novo Nordisk og Navamedic).
1. Folkehelseinstituttet. 2022 [Available from: https://www.fhi.no/nyheter/2022/de-fleste-har-overvekt-eller-fedme/.
2. Pi-Sunyer X, Astrup A, Fujioka K, Greenway F, Halpern A, Krempf M, et al. A Randomized, Controlled Trial of 3.0 mg of Liraglutide in Weight Management. New England Journal of Medicine. 2015;373(1):11-22.
3. Nissen SE, Wolski KE, Prcela L, Wadden T, Buse JB, Bakris G, et al. Effect of Naltrexone-Bupropion on Major Adverse Cardiovascular Events in Overweight and Obese Patients With Cardiovascular Risk Factors: A Randomized Clinical Trial. Jama. 2016;315(10):990-1004.
4. Davidson MH, Hauptman J, DiGirolamo M, Foreyt JP, Halsted CH, Heber D, et al. Weight Control and Risk Factor Reduction in Obese Subjects Treated for 2 Years With OrlistatA Randomized Controlled Trial. Jama. 1999;281(3):235-42.
5. Drucker DJ, Holst JJ. The expanding incretin universe: from basic biology to clinical translation. Diabetologia. 2023.
6. Tolentino J. Will the Ozempic Era Change How We Think About Being Fat and Being Thin? The New Yorker. 2023.
7. NRK. Slakemedisiner tar av [Available from: https://tv.nrk.no/serie/debatten/202304/NNFA51041323.
8. Statens_legemiddelverk. 2023 [Available from: https://legemiddelverket.no/import-og-salg/legemiddelstatistikk.
9. Wilding JPH, Batterham RL, Calanna S, Davies M, Van Gaal LF, Lingvay I, et al. Once-Weekly Semaglutide in Adults with Overweight or Obesity. New England Journal of Medicine. 2021;384(11):989-1002.
10. Garvey WT, Batterham RL, Bhatta M, Buscemi S, Christensen LN, Frias JP, et al. Two-year effects of semaglutide in adults with overweight or obesity: the STEP 5 trial. Nature medicine. 2022;28(10):2083-91.
11. Trujillo JM, Nuffer W, Smith BA. GLP-1 receptor agonists: an updated review of head-to-head clinical studies. Therapeutic Advances in Endocrinology and Metabolism. 2021;12:2042018821997320.
12. FDA. Guidance for Industry: Diabetes mellitus — evaluating cardiovascular risk in new antidiabetic therapies to treat type 2 diabetes. 2008 [Available from: http://www.fda.gov/downloads/Drugs/GuidanceComplianceRegulatoryInformation/Guidances/ucm071627.pdf.
13. Marso SP, Daniels GH, Brown-Frandsen K, Kristensen P, Mann JF, Nauck MA, et al. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. The New England journal of medicine. 2016;375(4):311-22.
14. Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jódar E, Leiter LA, et al. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. New England Journal of Medicine. 2016;375(19):1834-44.
15. Shimizu I, Hirota M, Ohboshi C, Shima K. Identification and localization of glucagon-like peptide-1 and its receptor in rat brain. Endocrinology. 1987;121(3):1076-82.
16. Turton MD, O’Shea D, Gunn I, Beak SA, Edwards CM, Meeran K, et al. A role for glucagon-like peptide-1 in the central regulation of feeding. Nature. 1996;379(6560):69-72.
17. Larsen PJ, Fledelius C, Knudsen LB, Tang-Christensen M. Systemic administration of the long-acting GLP-1 derivative NN2211 induces lasting and reversible weight loss in both normal and obese rats. Diabetes. 2001;50(11):2530-9.
18. Ard J, Fitch A, Fruh S, Herman L. Weight Loss and Maintenance Related to the Mechanism of Action of Glucagon-Like Peptide 1 Receptor Agonists. Adv Ther. 2021;38(6):2821-39.
19. Joly-Amado A, Cansell C, Denis RG, Delbes AS, Castel J, Martinez S, et al. The hypothalamic arcuate nucleus and the control of peripheral substrates. Best Pract Res Clin Endocrinol Metab. 2014;28(5):725-37.
20. Nauck MA, Meier JJ. Incretin hormones: Their role in health and disease. Diabetes Obes Metab. 2018;20 Suppl 1:5-21.
21. Hjerpsted JB, Flint A, Brooks A, Axelsen MB, Kvist T, Blundell J. Semaglutide improves postprandial glucose and lipid metabolism, and delays first-hour gastric emptying in subjects with obesity. Diabetes Obes Metab. 2018;20(3):610-9.
22. van Can J, Sloth B, Jensen CB, Flint A, Blaak EE, Saris WH. Effects of the once-daily GLP-1 analog liraglutide on gastric emptying, glycemic parameters, appetite and energy metabolism in obese, non-diabetic adults. Int J Obes (Lond). 2014;38(6):784-93.
23. Helsedirektoratet. [Available from: https://www.helsedirektoratet.no/rundskriv/kapittel-5-stonad-ved-helsetjenester/vedlegg-1-til–5-14-legemiddellisten/virkestoffer/naltrekson-og-bupropion?fbclid=IwAR1Rvh064QHA2uouqzNxcYFBwwyi6msSGC08whnz-e42QQ8RC5bm39Crs5o.
24. Felleskatalogen. 2021 [Available from: https://www.felleskatalogen.no/medisin/saxenda-novo-nordisk-658699#indikasjoner.
25. Lundgren JR, Janus C, Jensen SBK, Juhl CR, Olsen LM, Christensen RM, et al. Healthy Weight Loss Maintenance with Exercise, Liraglutide, or Both Combined. New England Journal of Medicine. 2021;384(18):1719-30.
26. Helsedirektoratet. Fysisk aktivitet 2023 [Available from: https://www.helsedirektoratet.no/tema/fysisk-aktivitet.
27. Bezin J, Gouverneur A, Pénichon M, Mathieu C, Garrel R, Hillaire-Buys D, et al. GLP-1 Receptor Agonists and the Risk of Thyroid Cancer. Diabetes care. 2023;46(2):384-90.
28. Novo_Nordisk. Wegovy, INN-semaglutide 2023 [Available from: https://www.novo-pi.com/wegovy.pdf#guide.
29. Jingi AM, Tankeu AT, Ateba NA, Noubiap JJ. Mechanism of worsening diabetic retinopathy with rapid lowering of blood glucose: the synergistic hypothesis 2017 [updated 2017/10/10. 63]. Available from: https://doi.org/10.1186/s12902-017-0213-3.
30. Cherney DZ, Tuttle KR. Liraglutide for the Treatment of Type 2 Diabetes and Safety in Diabetic Kidney Disease: Liraglutide and Diabetic Kidney Disease. Clin J Am Soc Nephrol. 2020;15(4):444-6.
31. Yang Z, Yu M, Mei M, Chen C, Lv Y, Xiang L, et al. The association between GLP-1 receptor agonist and diabetic ketoacidosis in the FDA adverse event reporting system. Nutr Metab Cardiovasc Dis. 2022;32(2):504-10.
32. Omar B, Ahrén B. Pleiotropic Mechanisms for the Glucose-Lowering Action of DPP-4 Inhibitors. Diabetes. 2014;63(7):2196-202.
33. Suran M. As Ozempic’s Popularity Soars, Here’s What to Know About Semaglutide and Weight Loss. Jama. 2023.
34. Wilding JPH, Batterham RL, Davies M, Van Gaal LF, Kandler K, Konakli K, et al. Weight regain and cardiometabolic effects after withdrawal of semaglutide: The STEP 1 trial extension. Diabetes Obes Metab. 2022;24(8):1553-64.