Pasienter som gjennomgår allogen hematopoietisk stamcelletransplantasjon har kompleks immunsvikt med risiko for en mengde ulike infeksjoner. Antiinfektiv profylakse har en viktig rolle, men infeksjonskomplikasjoner bidrar likevel til betydelig mortalitet, morbiditet og helsekostnader for pasientgruppen. Denne artikkelen gir en oversikt over de viktigste infeksjonene og oppfølging etter allogen hematopoietisk stamcelletransplantasjon.
Anders Eivind Myhre, Overlege, PhD. Avdeling for blodsykdommer, Oslo universitetssykehus
Ved allogen stamcelletransplantasjon mister pasienten all tidligere opparbeidet immunitet. Den kombinerte immunsvikten består av barrierebrudd (mukositt, sentralvenøs tilgang), agranulocytose, hypogammaglobulinemi, redusert antall og funksjon av T-celler samt immunhemmende medikamenter, som alle bidrar til økt infeksjonsrisiko. Mens pasienter transplantert med et solid organ vil trenge livslang immunsuppresjon, er målet etter allogen stamcelletransplantasjon å utvikle immunologisk toleranse og å fase ut all immunhemmende behandling etter tre til seks måneder. En stor andel av pasientene vil oppleve tilstrekkelig immunrekonstitusjon to til tre år etter transplantasjonen, men en ikke ubetydelig andel vil kun oppnå en delvis immunrekonstitusjon eller utvikle transplantat-mot-vert-sykdom (GvHD) med behov for langvarig immunhemmende behandling. Disse pasientene har betydelig økt risiko for opportunistiske infeksjoner og vil trenge regelmessig oppfølging i både primær- og spesialisthelsetjenesten.
Immunitet overføres til en viss grad fra donor til pasient ved at B- og T-hukommelseceller følger med under infusjonen av stamceller. Umiddelbart etter transplantasjonen vil donors immunceller være få og hemmet av immunsuppressiva, men vil over tid kunne ekspandere og gi tilstrekkelig immunitet, selv i fravær av reinfeksjon. Det er derfor en fordel å bruke en donor med kjent immunitet mot cytomegalovirus (CMV) og Epstein-Barr-virus (EBV) til en pasient som tidligere er smittet av disse virusene.
I hvilken grad T-cellene har mulighet til å ekspandere er avhengig av forskjellige faktorer, blant annet stamcellekilde (perifert blod, navlestreng, benmarg) og om T-celler er fjernet fra stamcelleproduktet eller sirkulasjonen for å forebygge GvHD. Pasienten kan utdanne nye T-celler, men voksne pasienter har redusert tymusfunksjon og har derfor begrenset kapasitet for dette.
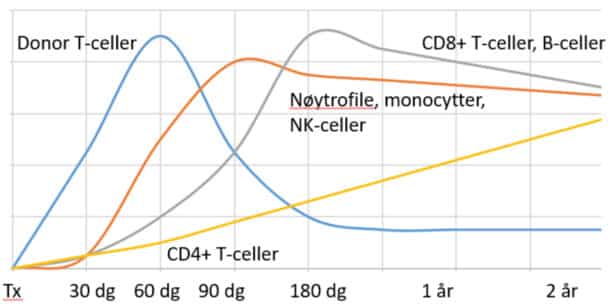
Immunsvikt og immunrekonstitusjon etter allogen stamcelletransplantasjon er en dynamisk tilstand, der utfordringer er avhengig av tid fra transplantasjonen, men også påvirkes i stor grad av tidligere behandling. Figur 1 skisserer typisk endring i leukocyttall i løpet av de første to årene etter transplantasjonen, og figur 2 viser hvordan infeksjonsrisikoen endrer seg over tid.

Det har vært utbredt praksis med isolering i overtrykksventilerte rom med spesiell luftfiltrering den første måneden, strenge kostrestriksjoner og regler for kjæledyr, barnehagebarn og sosial omgang. Evidensen for disse nokså inngripende tiltakene er sparsom, og de kan ha betydelig konsekvens for livskvalitet og evne til rekonvalesens (1). De senere år er isolasjonspraksisen løsnet opp, og i dag er basale hygieneprosedyrer og god opplæring av personell det viktigste tiltaket for de fleste pasientene, mens mer inngripende prosedyrer spares til de mest sårbare pasientene.
Risiko for bakterielle infeksjoner er størst de første tre-fire ukene etter transplantasjonen grunnet mukositt og agranulocytose forårsaket av kjemoterapi og/eller stråleterapi. Majoriteten av pasienter har i denne perioden feber. Oppvekst i blodkulturer sees i et mindretall av pasientene. De vanligste funn er gram-negative staver og enterokokker fra kolon, viridans-gruppe streptokokker fra munnhule og hvite stafylokokker fra hud og venøse katetre (2). Antibakteriell profylakse med et bredspektret fluorokinolon er utbredt internasjonalt, men det er ikke tradisjon for dette i Norge grunnet en velbegrunnet frykt for resistensutvikling. Kapittelet om behandling av febril nøytropeni i Helsedirektoratets retningslinjer for bruk av antibiotika i sykehus ble oppdatert i 2021. Penicillin/gentamicin er fortsatt standard behandling (3) også for pasienter som gjennomgår allogen hematopoietisk stamcelletransplantasjon.
Infeksjoner forårsaket av kapselkledde bakterier som Streptococcus pneumoniae og Haemophilus influenzae sees senere i forløpet hovedsakelig hos pasienter med vedvarende hypogammaglobulinemi (figur 2). Ved residiverende infeksjoner med kapselkledde bakterier eller dokumentert hypogammaglobulinemi anbefales immunglobulin-substitusjon.
Insidensen av invasive soppinfeksjoner etter allogen stamcelletransplantasjon er høy, og har vært gjennomsnittlig 20% ved Oslo universitetssykehus de siste ti årene (4). Varigheten av agranulocytose og bruk av systemiske kortikosteroider er de viktigste risikofaktorene (5). Risikoen er størst den første måneden etter transplantasjon, men også senere i forløpet hos pasienter med GvHD. Gjærsopp, hovedsakelig Candida albicans er dominerende agens, mens andel muggsoppinfeksjoner er økende og nærmer seg halvparten av infeksjonene. Aspergillus sp. (oftest A. fumigatus) er det vanligste muggsoppagens, men andre muggsoppinfeksjoner, blant annet mucormykose, er økende (4). Mucormykose responderer dårlig på antimykotisk behandling, og det kreves ofte omfattende kirurgi for å få infeksjonskontroll. Den totale insidensen for invasive soppinfeksjoner ser ut til å være noe fallende, antageligvis fordi alle pasienter mottar profylakse med et triazol (flukonazol eller posakonazol). Overlevelsen ved etablert infeksjon er blitt bedre, og bedret diagnostikk og behandling bidrar trolig til dette.
Pneumoni forårsaket av Pneumocystis jirovecii (PCP) forekommer oftest senere i forløpet (ofte seks måneder til to år etter transplantasjonen), i tilfeller hvor pasienten enda ikke har oppnådd tilstrekkelig T-celle-funksjon. Profylakse med trimetoprim/sulfametoksazol gis fra stabil benmargsfunksjon, vanligvis fire til seks uker etter transplantasjonen, til pasientene har avsluttet systemisk immunsuppresjon og CD4-tall er over 200 x106/L, som regel minst seks måneder etter transplantasjonen. Dapson, pentamidin-inhalasjoner eller atovakvon kan benyttes ved dårlig benmargsfunksjon eller intoleranse for trimetoprim/sulfametoksazol (6).
Reaktivering av herpesvirus er en viktig komplikasjon ved stamcelletransplantasjon. Lymfopeni og immunhemmende medikamenter er de viktigste risikofaktorene og kan vedvare i flere år. Før rutineprofylakse ble innført var disseminerte infeksjoner med herpes simplex- (HSV) eller varicella zoster-virus (VZV) vanlige problem, men forekommer nå sjeldent (7). Profylakse med aciklovir eller valaciklovir anbefales i minst ett år etter transplantasjonen for alle som er seropositive for varicella zoster, noe svært få voksne pasienter ikke er. Noen pasienter vil etter seponering oppleve tilbakevendende HSV-reaktivering og vil dermed trenge profylaktisk behandling på ubestemt tid, mens VZV-reaktiveringer oftest skjer bare én gang.
I underkant av 70% av voksne norske pasienter er seropositive for CMV, og halvparten vil oppleve CMV-reaktivering i løpet av de fire første månedene (4) etter transplantasjonen. Organaffeksjon, spesielt pneumoni, kolitt og retinitt, forhindres i stor grad ved å systematisk monitorere viremi og sette inn behandling før klinisk sykdom oppstår (preemptiv behandling) (8). CMV-DNA i plasma analyseres minst én gang i uken når enten pasient eller donor er CMV-seropositive. Ved påvist viremi startes ganciklovir/valganciklovir eller foskarnet, men behandlingen er forbundet med betydelige bivirkninger, spesielt tidlig etter transplantasjonen. Profylakse med letermovir kan forhindre tidlig reaktivering og har vist overlevelsesgevinst i en stor klinisk studie (9).
EBV-reaktivering var tidligere sjelden, men forekomsten har økt betydelig etter at flere pasienter nå behandles med antitymocytt immunglobulin (T-celledeplesjon) for å forebygge GvHD. EBV kan både forårsake et hyperinflammatorisk syndrom og post-transplantasjons lymfoproliferativ sykdom. Monitorering av EBV-viremi og preemptive tiltak kan redusere risikoen for alvorlig forløp. Tiltakene er reduksjon av immunhemmende behandling og eventuelt B-celledepleterende behandling (CD20-antistoff, rituksimab) (10).
Reaktivering av polyomavirus (først og fremst BK-virus, sjelden JC-virus) og humant herpesvirus-6 kan gi hemorragisk cystitt (BKV) og encefalitt (JCV, HHV6). Effektive strategier for profylakse eller preemptiv behandling finnes ikke (7). Viktigste tiltak for å forhindre disse infeksjonene er å unngå unødvendig langvarig og intensiv immunhemmende behandling.
Adenovirus-infeksjon forekommer relativt hyppig hos barn, sjeldnere hos voksne, gir oftest kolitt, er som regel forårsaket av nysmitte, men kan også reaktiveres fra bærertilstand (7).
Reaktivering fra bærertilstand av viral hepatitt, hovedsakelig hepatitt B, er en relevant problemstilling, men sees heldigvis sjelden ved bruk av profylakse med entekavir eller tenofovir (11).
Infeksjoner med vanlige luftveisvirus forekommer hyppig hos transplanterte, som i befolkningen ellers. I de aller fleste tilfellene er forløpene milde, men alvorlige infeksjoner med influensavirus, parainfluensavirus, RS-virus, metapneumovirus, koronavirus med flere forekommer. Risikoen for alvorlig forløp og død av Covid-19-infeksjon er rapportert å være betydelig forhøyet (12), men smittebølgen med omikron-varianten som rammet pasienter i Norge vinteren og våren 2022 ga i hovedsak mild sykdom.
Rundt 10% av befolkningen har latent infeksjon med parasitten Toxoplasma gondii som kan gi reaktiveringer med encefalitt og pneumonitt, nesten alltid i løpet av de første tre til seks månedene etter transplantasjonen. En sjelden gang sees også primærinfeksjon etter inntak av utilstrekkelig varmebehandlet kjøtt. Profylakse med trimetoprim/sulfametoksazol mot PCP gir også effektiv beskyttelse mot toksoplasmose, og reaktivering sees hovedsakelig hos pasienter som får alternativ eller ingen PCP profylakse (13).
Etter hematopoietisk stamcelletransplantasjon bør pasienten for alle praktiske formål oppfattes som uvaksinert. Vaksinasjonsprogrammet er av stor nytte for pasienten, siden det finnes trygge og effektive vaksiner mot blant annet pneumokokker, influensa og hepatitt B (14). Revaksinasjon mot difteri, stivkrampe, kikhoste, poliomyelitt, og Haemophilus influenzae serotype B anbefales fra seks måneder etter transplantasjonen. Revaksinasjon med Covid-19-vaksine startes tre måneder etter transplantasjonen, og revaksinering med totalt fire doser anbefales.
Grunnet økt risiko for systemisk pneumokokksykdom anbefales tre doser pneumokokk konjugatvaksine fra tre måneder etter transplantasjonen. Hos pasienter med GvHD anbefales ytterligere en dose konjugatvaksine 12 måneder etter transplantasjonen, mens polysakkarid-vaksine anbefales til andre. Årlig influensavaksine anbefales med start fra fire måneder etter transplantasjonen.
Levende vaksiner er som hovedregel kontraindisert, men kan tilbys pasienter som to år etter transplantasjonen ikke har GvHD eller bruker immunsuppresjon. Varicellavaksine (Varivax eller Varilrix) er aktuelt til pasienter som ikke har gjennomgått vannkopper eller ikke har antistoffer mot varicella zoster virus. Zostavax skal ikke brukes, mens sikkerhet og effekt av den rekombinante zoster-vaksinen (Shingrix) foreløpig ikke er godt nok dokumentert i denne pasientgruppen. Vaksine mot meslinger (MMR) er aktuelt hos pasienter som ikke har antistoffer mot morbillivirus,
Folkehelseinstituttets vaksinasjonsveileder er oppdatert i 2022 for immunsvikt, inkludert stamcelletransplantasjon (15). Vaksinasjonene utføres i primærhelsetjenesten. Anbefalte vaksiner er refundert via blåreseptordningen §4. Unge kvinner vil miste beskyttelse mot humant papillomavirus (HPV) og kan ha nytte av ny HPV vaksinering. Inntil videre er dessverre kostnader for revaksinering med HPV-vaksine ikke dekket av noen refusjonsordninger.
Infeksjoner er, sammen med GvHD, den hyppigste årsaken til behandlingsrelaterte komplikasjoner og dødsfall hos pasienter etter allogen stamcelletransplantasjon. Identifikasjon av risikopasienter, riktig bruk av medikamentell profylakse, monitorering av relevante agens, rask og omfattende utredning, bred empirisk behandling og innsmalning etter påvist infeksjon, er alle sentrale elementer i en vellykket stamcelletransplantasjon. Økende forekomst av resistente bakterier og sopp er en vesentlig utfordring, både i dag og for fremtiden. Vaksinering etter transplantasjon er viktig for å forhindre allmennfarlige smittsomme sykdommer.